イオン透過
「細胞膜におけるイオンの選択的透過の機構」
■背景
我々の体液は電解質(イオン)を含む水溶液です。イオンは普段は細胞の内外を出入りできませが、細胞膜にはイオンチャネルと呼ばれる「穴」があります。これは外からの刺激(例えば、匂いを感じた時、物に触れた時)に応じて開閉し、この穴が開いた時にのみ、イオンはチャネルを通って細胞内外を出入りできます。これによって「匂いを感じた(嗅覚)」「物に触れた(触覚)」という感覚が生まれるのです。さらに、脳で物事を考えたり、筋肉を動かすためにも細胞内外でのイオンの出入りは不可欠なのです。
このイオンの出入りを「イオン透過」と言います。また、イオンチャネルには種類があり、ナトリウム(Na+)イオンをよく通すチャネルをNa+チャネル、カリウム(K+)イオンをよく通すチャネルをK+チャネルと呼びます。つまり、チャネルはNa+やK+などのイオンを選んで透過させており、これを「選択性」と言います。
イオンの選択的透過の機構を解明するための研究は80年以上も続けられており、3度のノーベル賞が授与されています(1963年生理学・医学賞、1991年生理学・医学賞、2003年化学賞)。また、温度や触覚のセンサーもイオンチャネルであり、その発見に対してもノーベル賞が授与されています(2021年生理学・医学賞)。
現代では、スーパーコンピュータを使ってシミュレーションをすることで、イオンがチャネルを透過する様子を映した動画を作ることができます(図1)。この動画を調べることで近年解明されつつあるK+チャネルにおける選択的透過の機構を説明します。
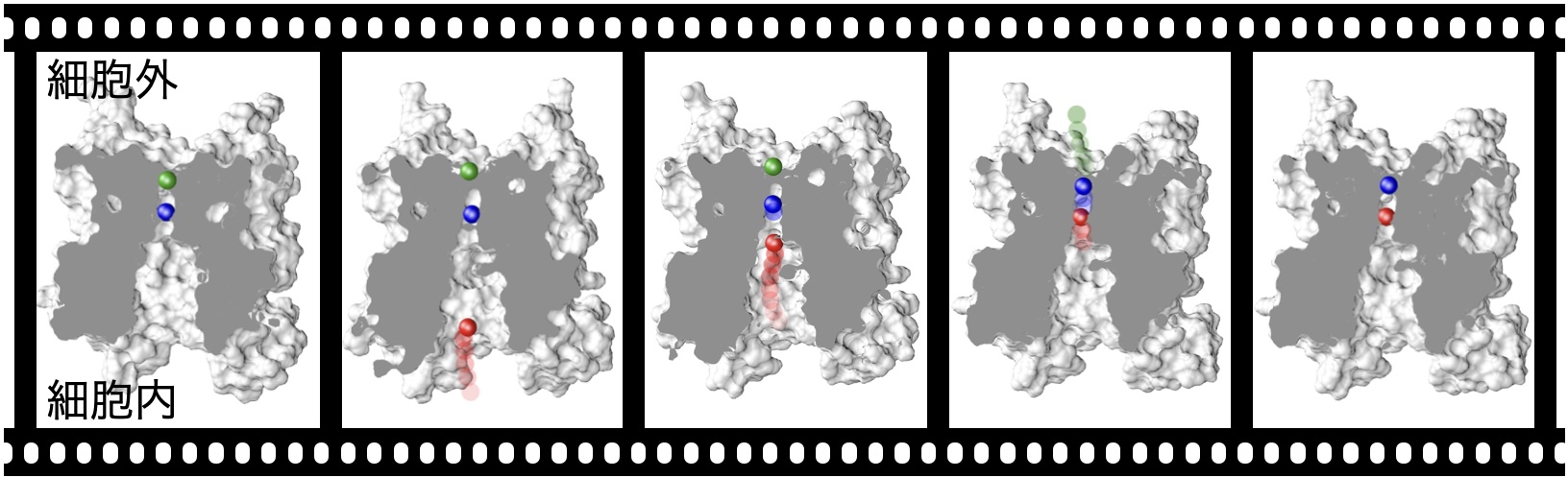
図1 K+チャネルの断面とK+イオン(赤、青、緑の球)が透過する動画。紙面上が細胞外、下が細胞内溶液である。
■研究概要
これまでK+チャネルの選択性は高いと考えられており、多くの教科書には「Na+に対して10,000倍もK+は透過する」と書かれています。しかし、シミュレーションをすると、驚くことに約40倍の選択性しかなく、電気生理学実験によっても約80倍であることが確認されました(文献1)。つまり、想定されていたほど選択性は高くないのです。
また、K+チャネルでの選択性は高いため、「K+イオンとK+チャネルは強く引き合う」と考えられていました。「強く引き合う」のであれば、一度K+チャネルに入ったK+イオンは、なかなか出られないと考えられます。しかし、電気生理学実験によれば、1秒間に1億個ものK+イオンが透過することも分かっていました。強く引き合うにも関わらず多量のイオンが透過できるのはなぜか?
この疑問を解決するため科学者が長く信じていた透過機構は、ノックオン機構と呼ばれるものです。これは「チャネルと強く引き合っているイオンを、次にチャネルに入るイオンがクーロン力で弾き出す」つまりビリヤードのような機構です(文献2)。しかし、実は強く引き合っていないことが分かった今、ノックオン機構とは異なる透過の仕方もあるはずです。実際、シミュレーションによって、ノックオン機構により押し出される前にチャネルの中のイオンが流れ出てしまう場合があることも観察されており、このような新しい透過機構は待ち行列機構と呼ばれています(図2、文献3、4)。また、待ち行列機構を裏付ける結果も電気生理学実験により得られています(文献5)。
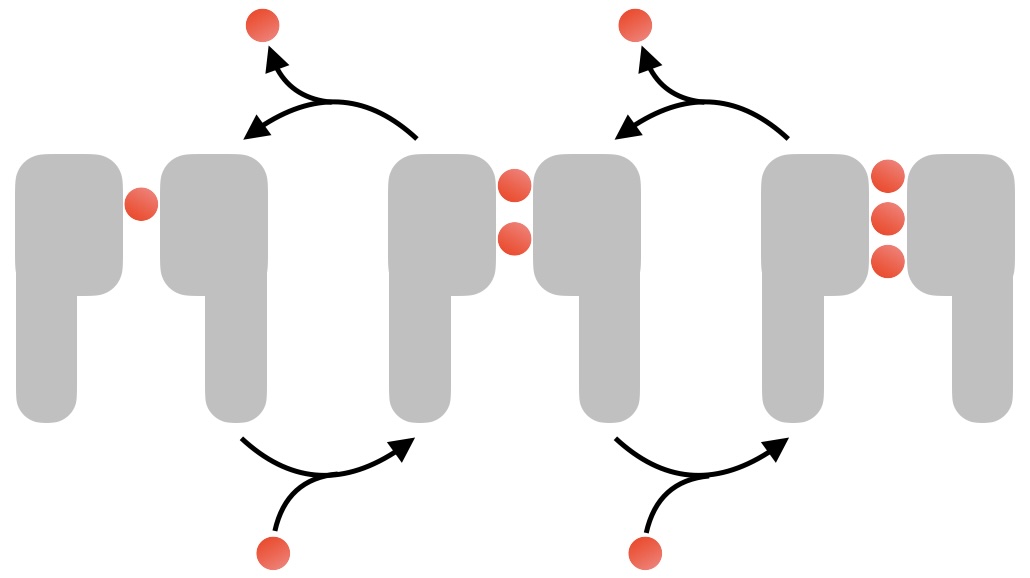
図2 待ち行列機構。K+チャネルを灰色の模式図で、K+イオンを赤の球で表している。K+イオンは、買い物のレジで店員(K+チャネル)の会計処理を待つ客の行列と似ている。次の客が行列に並ぶ前に会計が終わる場合、列(K+チャネル内のK+イオンの個数)は小さくなる。電気生理学実験からは、K+チャネルにK+イオンが全く存在しない場合があることも示唆されている(文献5)。
■科学的・社会的意義 感覚や思考を生み出す分子であるイオンチャネルでのイオンの選択的透過機構の解明は、多数のノーベル賞授与からも分かる通り、極めて重要な基礎科学の研究です。医学的には、K+チャネルでのイオン透過速度の増強によるT細胞のガン細胞攻撃能を回復させる薬の開発が行われており、社会的意義もある研究と思われます。一方、科学は日進月歩であり、ここで紹介した機構よりも確からしい機構があるかもしれません。読者の中から、そのような機構を提案する人材が生まれることを願っています。
■参考文献
1)K. Mita, T. Sumikama, et al. (2021). “Conductance selectivity of Na+ across the K+ channel via Na+ trapped in a tortuous trajectory.” Proc Natl Acad Sci USA 118: e2017168118.
2)A. Mironenko, U. Zachariae, B. L. de Groot, W. Kopec (2021). “The Persistent Question of Potassium Channel Permeation Mechanisms.” J Mol Biol 433: 167002.
3)T. Sumikama, S. Oiki (2016). “Digitalized K+ Occupancy in the Nanocavity Holds and Releases Queues of K+ in a Channel.” J Am Chem Soc 138: 10284-10292.
4)T. Sumikama, S. Oiki (2019). “Queueing arrival and release mechanism for K+ permeation through a potassium channel.” J Physiol Sci 69: 919-930.
5)M. Iwamoto, S. Oiki, (2011). “Counting ion and water molecules in a streaming file through the open-filter structure of the K channel.” J Neurosci 31: 12180-12188.
 R6年度分野別専門委員
R6年度分野別専門委員
金沢大学・ナノ生命科学研究所
炭竈享司 (すみかまたかし)
https://www.researchgate.net/profile/Takashi-Sumikama
「生体膜におけるイオン選択的透過の謎に迫る」
■背景 私たちの細胞膜にはイオンチャネルと呼ばれるタンパク質が存在し、細胞膜を貫通する穴を作ることでイオンの通り道となっています。実はこの穴は単なる「穴」ではなく、真似しても到底作ることのできない「高効率フィルター」なのです。例えば、1分子のカリウムイオンチャネルはカリウムイオンを1秒間に1000万個以上のスピードで通すことができますが、カリウムイオンよりも少しだけ小さなナトリウムイオンはほとんど通しません。私たちの細胞膜に存在するたくさんのイオンチャネルにはこの様なイオン選択性があり、そのおかげで細胞内外のイオンバランスが維持され、時にこの「穴」が開閉することで様々な情報伝達信号が作られているのです(図1)。
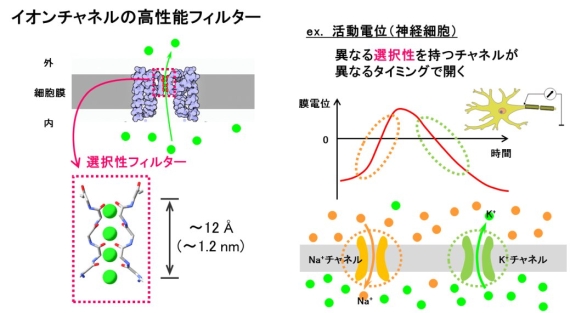
図1.イオンチャネルタンパク質の構造と神経細胞での機能(電気信号発生)の例
■研究概要 それでは、イオンチャネルの高性能フィルターにはどのような仕組みがあるのでしょうか?膜電流測定という非常に感度の高い測定法を用いれば、イオンチャネルの機能とその変化を刻一刻と追跡することができます。わずか1分子のイオンチャネルを流れるイオンの流れ(=電流)も比較的容易に観測することが可能です(図2)。ここで観測される単一チャネル電流には、イオンチャネルのフィルター内をイオンが透過していく際に発せられる様々な情報が暗号のように組み込まれています。我々は、膜電位、イオン濃度、浸透圧など、イオンチャネル周囲の環境が単一チャネル電流へ及ぼす影響を手掛かりに、この暗号の解読を試みています。最近の成果の1つとして、チャネル内をイオンはランダムに通っているのではなく、水分子と交互に規則正しく1列に並んで通過していることを明らかにしました。実は、イオンの選択的透過機構には水分子が欠かせない存在だったのです(図3,文献1,3)。この現象の更なる理解に向け、数学的解析(文献2)や遺伝子工学的手法を組み合わせ、多面的にイオン透過を捉える試みを行っています。
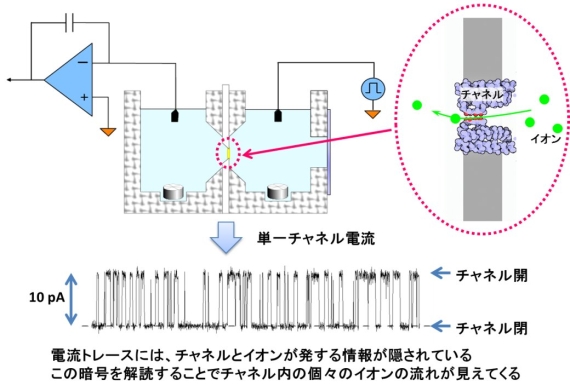
図2.脂質平面膜法による単一チャネル電流測定
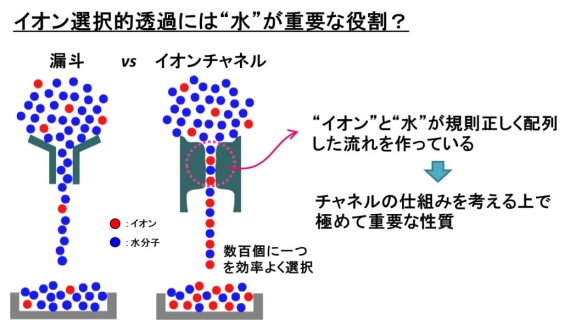
図3.イオンチャネル内のイオン選択的透過には水が欠かせない
■科学的・社会的意義 生体膜でのイオン選択的透過は、多くの生体反応の本質を担う重要な生理現象です。しかしそのメカニズムは、分子レベルでは意外なほど明らかになっていません。我々の研究を含めイオン透過に関する多くの研究は、この未解決の難問に対して様々な角度からアプローチする役割を担っています。また、イオンチャネルのイオン選択性喪失によって引き起こされる疾患も最近明らかになってきています。このような疾患の原因をより深く理解することは、治療法や薬の開発にも役立つ可能性があります
■参考文献
1)M. Iwamoto, S. Oiki (2011). "Counting ion and water molecules in a streaming file through the open-filter structure of the K channel" J.Neurosci. 31, 12180-12188.
2)S. Oiki, M. Iwamoto, T. Sumikama (2011). "Cycle flux algebra for ion and water flux through the KcsA channel single-file pore links microscopic trajectories and macroscopic observables" PLoS ONE 6: e16578.
3)老木成稔,安藤博之,久野みゆき,清水啓史,岩本真幸 (2008). “Kチャネルのイオン透過機構:新しい流動電位測定法により明らかになったイオン-水流束比” 生物物理48, 246-252.
■良く使用する材料・機器
1)単一チャネル電流測定装置 Axopatch 200B, Digidata 1440A(Molecular Devices)
2)倒立型顕微鏡 IX71(オリンパス)
3)電動マニピュレータ MP-285(Sutter Instrument)
4)合成リン脂質(Avanti Polar Lipids)
5)実験試薬(ナカライテスク)
 H24年度分野別専門委員
H24年度分野別専門委員
福井大学医学部・分子生理学
岩本真幸 (いわもとまさゆき)
https://seiri1.med.lab.u-fukui.ac.jp/ja
