細胞運動
「車輪細胞のアメーバ運動をおもちゃロボットから考えてみた」
■背景
細胞運動は、胚の発生や免疫応答、傷の修復など細胞の重要な機能の一つです。細胞運動の様式の一つに基盤に接着して這い回る広義のアメーバ運動があります。魚の表皮に傷が生じると、傷周囲の表皮細胞ケラトサイトがアメーバ運動で移動し修復します。移動中のケラトサイトの細胞体はちょうど空気が抜けて底面が潰れたラグビーボールのような形をしていて回転しています(文献 1, 2)。ラグビーボールの縫い目に沿うようにストレスファイバと呼ばれる筋肉のように収縮する繊維が並んでいます(図1)。私たちは2018年にストレスファイバが細胞体の回転に必要なことを見つけ、車輪細胞として発表しました(文献 3)。しかし、ストレスファイバの直線的な収縮がどうやって回転運動に変換されるのか、は謎のままでした。
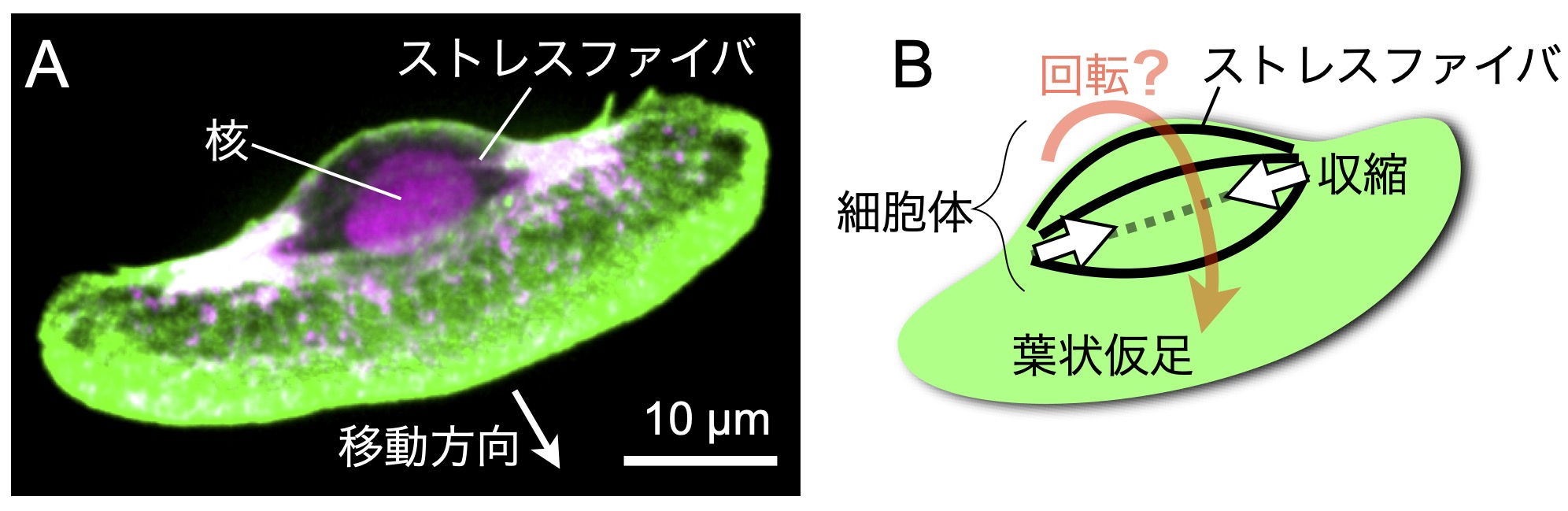
図1 魚類表皮細胞ケラトサイト。A:蛍光画像。緑が F-actin、マゼンタが myosinⅡ。B:模式図。
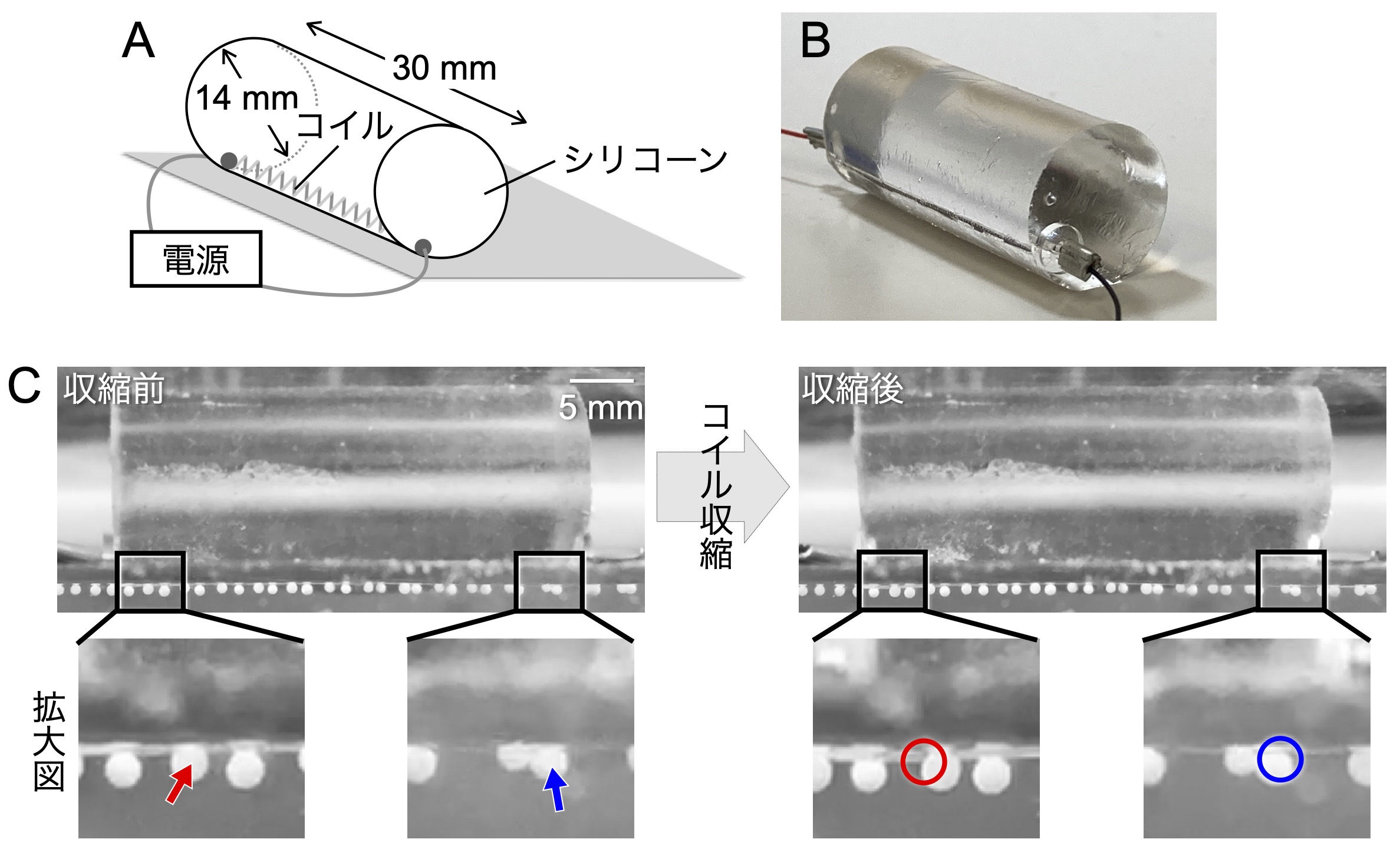
図2 おもちゃロボット。A:模式図。B:写真。C:おもちゃロボットが基盤を押す。やわらかい基盤表面に埋め込まれたビーズのうち、シリコーン円柱両端付近のもの(矢印)がコイルの収縮によって沈む。丸印は収縮前の矢印で示したビーズの位置。
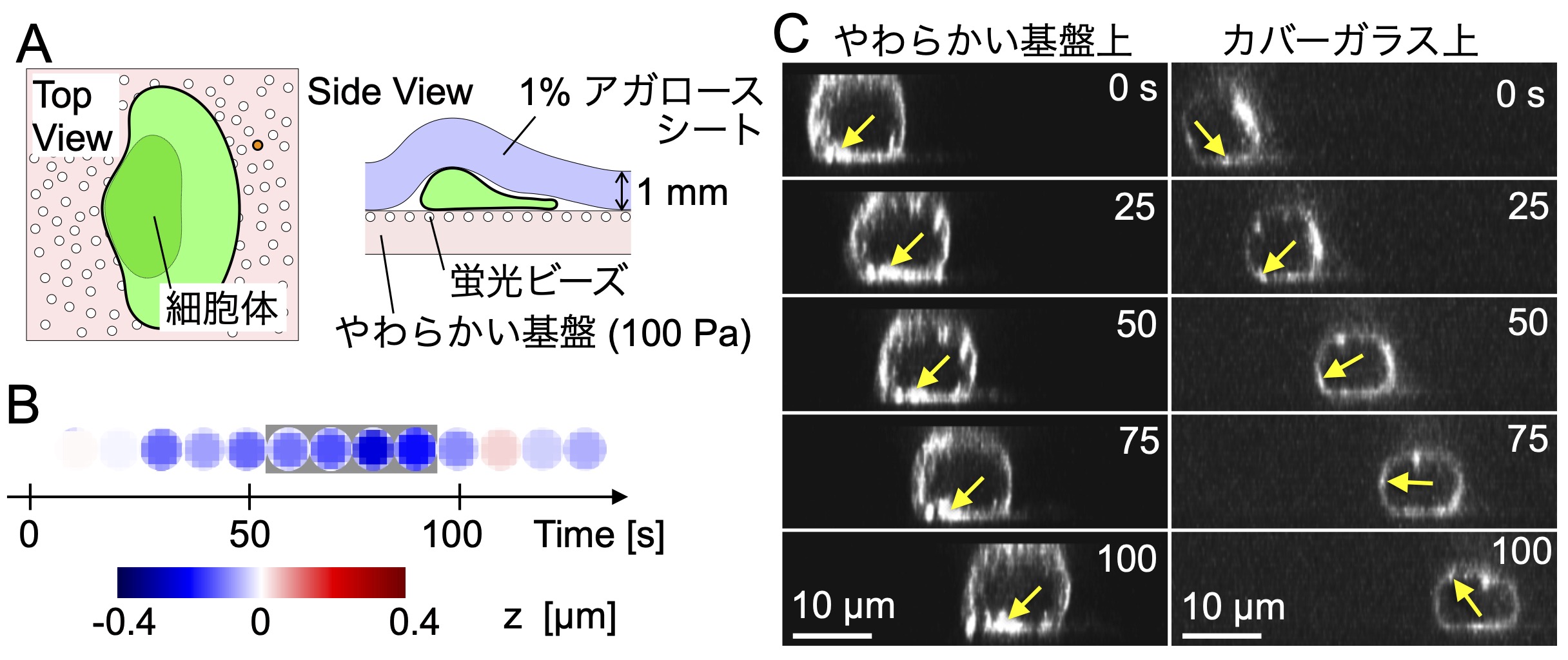
図3 ケラトサイトの観察。A:模式図。B:特定の蛍光ビーズ(Aのオレンジに相当)のz方向の変異。細胞体左端の通過時(グレー)に凹む。C:ストレスファイバの回転の断面図。矢印:ストレスファイバ。カバーガラス上の細胞では回転するがやわらかい基盤上では回転しない。
■研究概要 この謎に答えるため、私たちはケラトサイトの細胞体を模したおもちゃロボットを作製しました(図2)。ストレスファイバに相当するコイルを収縮させると、なんとロボットは回転したのです。そこで、どうやってこのロボットは回転するのか、その動作原理を大真面目に検討しました。ロボットの回転原理からケラトサイトの細胞体の回転メカニズムが予言できると思ったからです。果たしてロボットでは、コイルの収縮でシリコーン円柱が変形し、基盤を押して回転していました。同じ仕組みがケラトサイトで機能しているかどうか、生細胞のライブイメージングで観察しました(図3)。すると、たしかにケラトサイトでもストレスファイバの収縮が細胞体を変形させ、変形した細胞体が地面を押して回転していたのです(文献 4)。直動回転変換は人工機械で古くからみられる重要な機構です。100年以上の歴史のあるエンジンでさえ、ピストンの直線運動を回転運動に変換するためには、コネクティングロッドやクランクシャフトなど複雑な機構を必要としています。しかし、細胞はそんな複雑な機構を持ちません。その代わり柔軟性を持っています。ケラトサイトは人工機械にはないやわらかいという生命独特の性質を利用して直動回転変換を実現していました。
■科学的・社会的意義 私たちの研究は、生命が単純なメカニズムでいとも簡単に直動回転変換を実現していたという自然科学の驚きであるとともに、素材の柔らかさを利用した新しいバイオミメティクスへの発展も期待できます。
■参考文献
1)Anderson, K.I., Wang, Y.L., and Small, J.V. (1996). Coordination of protrusion and translocation of the keratocyte involves rolling of the cell body. J. Cell Biol. 134, 1209–1218.
2)Svitkina, T.M., Verkhovsky, A.B., McQuade, K.M., and Borisy, G.G. (1997). Analysis of the actin-myosin II system in fish epidermal keratocytes: mechanism of cell body translocation. J. Cell Biol. 139, 397–415.
3)Okimura, C., Taniguchi, A., Nonaka, S. and Iwadate, Y. (2018). Rotation of stress fibers as a single wheel in migrating fish keratocytes. Sci. Rep. 8: 10615.
4)Okimura, C., Akiyama, S., Nishigami, Y., Zaitsu, R., Sakurai, T. and Iwadate Y. (2025). Linear contraction of stress fibers generates cell body rotation. Cell Rep. Phys. Sci. 6: 102429.
■良く使用する材料・機器
1) 倒立顕微鏡システム Ti-2 (株式会社ニコン)
2) 共焦点ユニットCSU-W1 (横河電機株式会社)
3) EMCCDカメラ iXon Life (アンドール)
 2025年分野別専門委員
2025年分野別専門委員
山口大学大学院・創成科学研究科
沖村千夏 (おきむらちか)
http://biophysics.sci.yamaguchi-u.ac.jp/
「小さな生命体はどのような仕組みで動くのだろう?」
■背景
細菌は、この地球上でもっともたくさん存在する生命体です。1匹のサイズは1ミリの1/1000ほどしかありませんが、1匹1匹が自由自在に動き回ることができます。この動きの中に生きものらしさを感じずにはいられません。生命科学において、もっとも重要な問いかけは「生命とは何か?」です。小さな生命体が、なぜ・どのように動くのか調べることで、生命の秘密を解き明かすことができます。
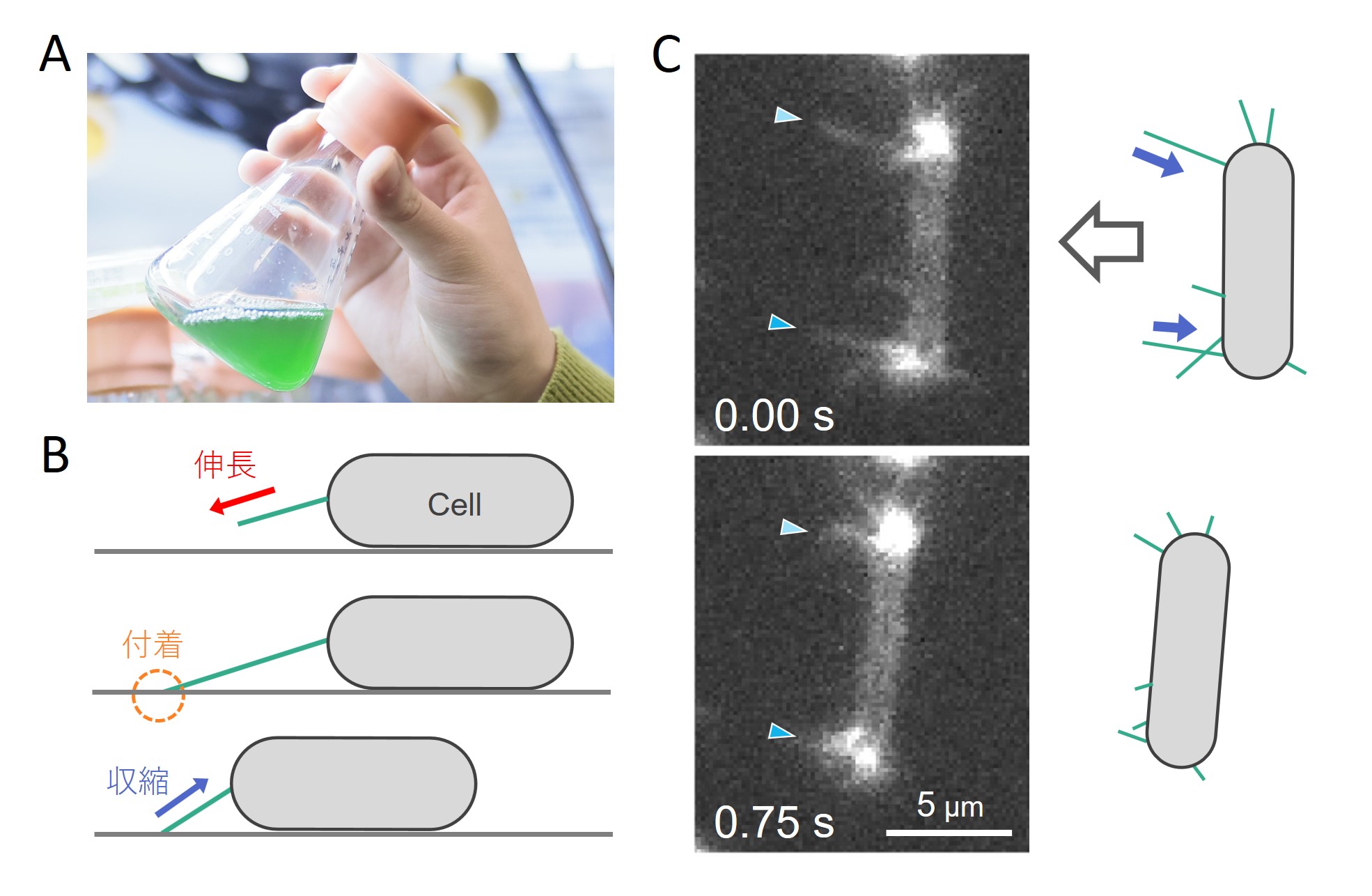
図1 藍藻の一種であるサーモシネココッカスの動き。(A) 細菌の培養液。緑色をしており、光合成をする。(B) 細菌の動きを横から見た模式図。ガラスなどの表面に付着し、細い糸を伸長、付着、収縮を繰り返することで、自身の体を前に進める。(C) 細菌の動きを上から観察した顕微鏡像。矢頭で示した細い糸が収縮することで、左方向に移動している様子をとらえた。
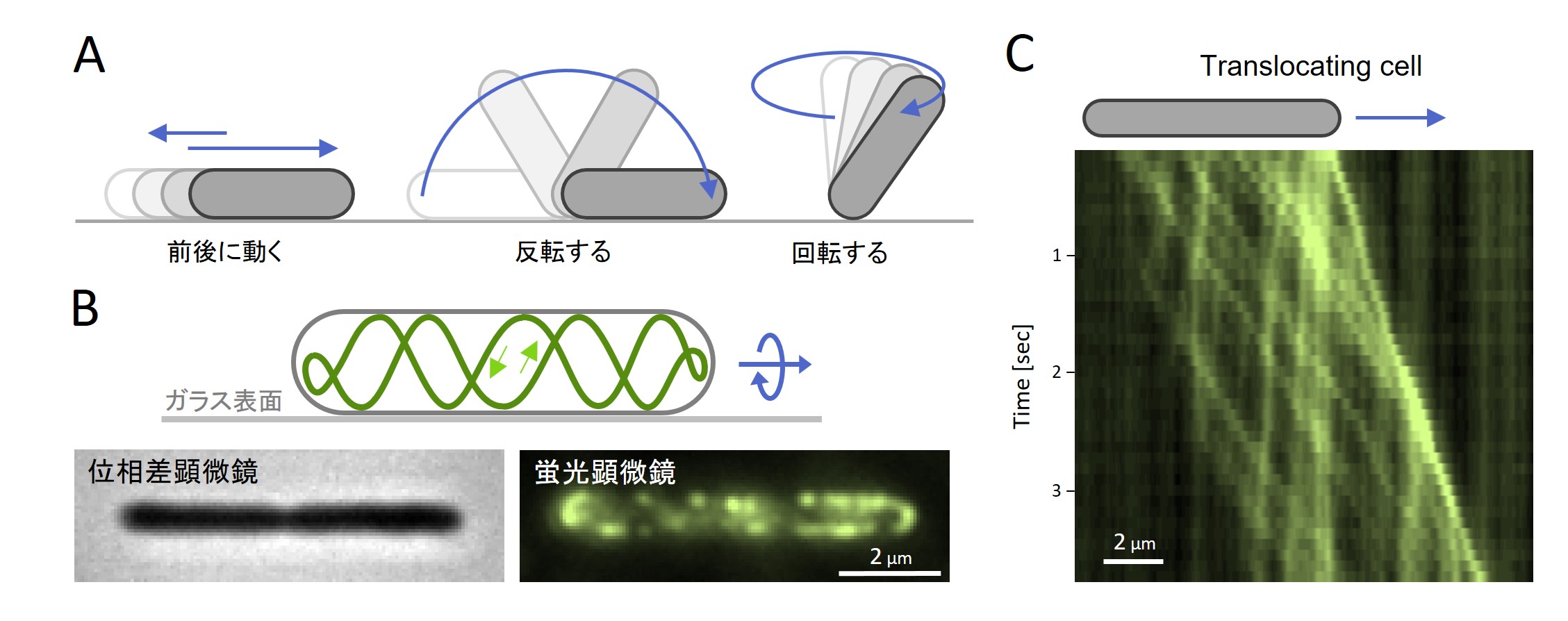
図2 土壌細菌であるフラボバクテリアの動き。(A)ガラスなどの固形物表面じょうを前後に動くだけでなく、反転したり、回転したりする複雑なふるまいを見せる。(B) この細菌を位相差顕微鏡で観察すると棒状のかたちをもつ。表面にある付着タンパク質を蛍光顕微鏡で観察すると細胞全体にまだらに局在している。この付着タンパク質が体の表面をぐるぐるとキャタピラのように動き回ることで推進力が発生する。(C) 付着タンパク質の動きを光学顕微鏡で観察し、キモグラフにより解析した。縦軸が時間。横軸が付着タンパク質の位置。動きに規則性があるのがわかる。
■研究概要 では、細菌はどのように泳ぐのでしょうか?私たちヒトのような手足を持たないため、泳ぎ方も全く異なります。一般的には、細菌はべん毛という繊維をスクリューのように毎秒100 回ほど高速回転させることで推進力を発生します(項目A-11 バクテリアべん毛の記事を参照)。ところが、淡水に生息する藍藻の多くはスパイダーマンのように細い糸を伸縮させることで移動します(図1、文献1)。土壌細菌であるフラボバクテリアは、自分の体の表面をキャタピラのようにぐるぐると回転させて移動します(図2、文献2)。私は光学顕微鏡にちょっと工夫をすることで、この動態を可視化することに日々挑戦しています。
■科学的・社会的意義 細菌の運動の研究は、細菌の生き残り戦略や生命の本質を理解するだけでなく、細菌運動を模した機械や素材の開発など、応用面にも貢献する可能性があります。
■参考文献
1)Nakane D, Enomoto G, et al. (2022). " Thermosynechococcus switches the direction of phototaxis by a c-di-GMP-dependent process with high spatial resolution" eLife 11: e73405.
2)Nakane D, Sato K, et al. (2013). "Helical flow of surface protein required for bacterial gliding motility." PNAS 110: 11145-50.
■良く使用する材料・機器
1) 倒立顕微鏡 IX73 (エビデント/オリンパス)
2) 光学フィルター (クロマテクノロジジャパン)
3) sCMOSカメラ Zyla (アンドール)
 2024年分野別専門委員
2024年分野別専門委員
電気通信大学・基盤理工学専攻
中根大介 (なかねだいすけ)
https://nakane-lab.amebaownd.com/
「細胞の物理的な制御からその運動の巧妙さに迫る」
■背景 生物は発生における複雑な形態の形成や、規則正しい運動様式などさまざまな調和を生み出すことができます。これは運動している細胞も同じです。アメーバ運動している細胞は前後極性を自分で決めているし(図1A)、特定の形になって運動する細胞もいます(図1B)。繊毛やべん毛を使って泳いで移動する細胞(図1C)は、それぞれの繊毛・べん毛を規則正しく動かすことで効率良く泳ぐことが出来ます。ゾウリムシ(図2A)を例にもうちょっと詳しく考えてみましょう。ゾウリムシはどこの池にもいる単細胞生物で、全身が多数の繊毛に覆われています。これら繊毛1本1本が発生する推進力で細胞が前進します。それぞれの繊毛がテンデンバラバラに動いていては効率よく泳げそうにありません。実は、それぞれの繊毛は隣り合う者同士がわずかな時間差で打っているのです。そうすると、繊毛打はきれいな波となって全身に伝わります。この波をメタクロナール波と呼びます(図2B)。神経もない単細胞のゾウリムシがどうやって全身の細胞を一定の時間差で打ち続けることができるのでしょう?
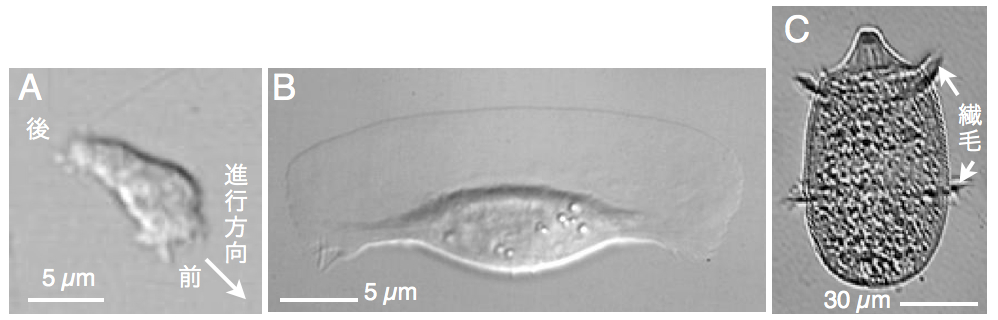
図1 運動している細胞達。A:筆者の血液の好中球。B:魚類表皮細胞ケラトサイト。C:カメガタヌマミズケムシ Didinium nasutum。
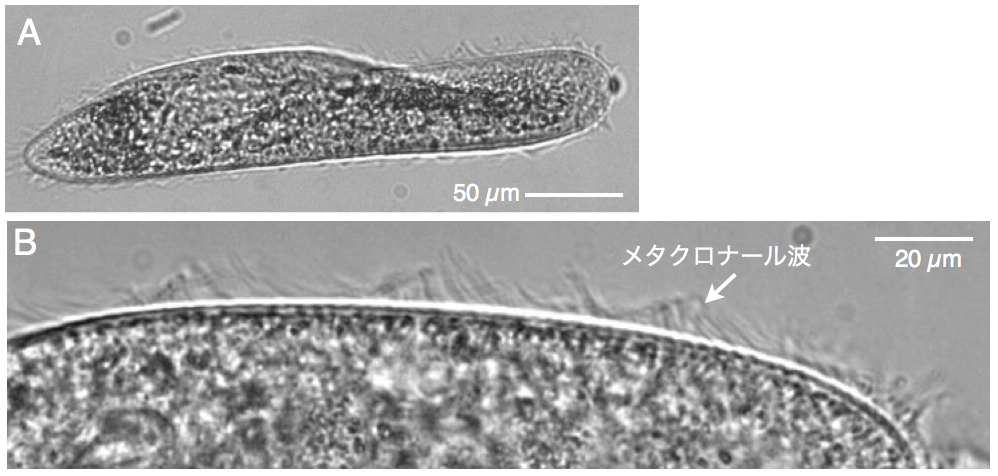
図2 ゾウリムシ Paramecium caudatum。A:全体像。B:拡大図。隣り合う繊毛がわずかな時間差で打つことで繊毛打が波となって伝わる。
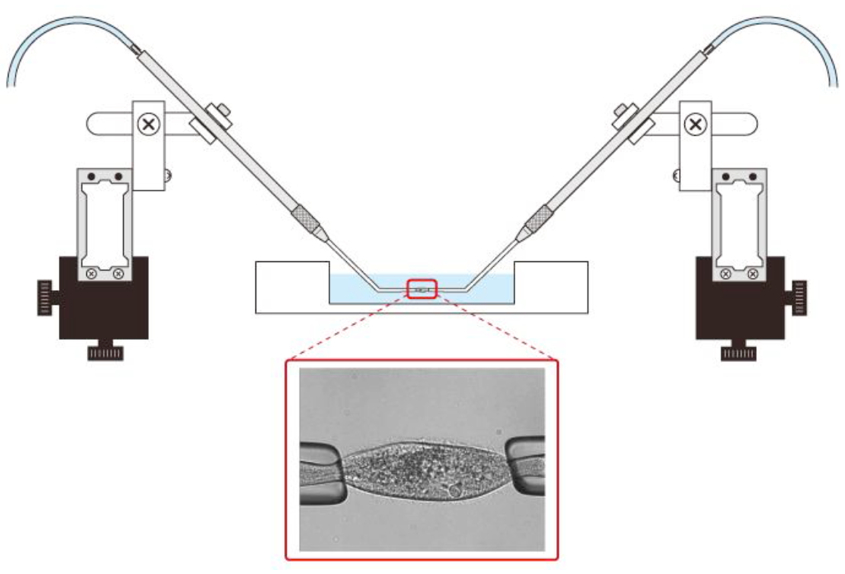
図3 ゾウリムシの強制的な伸縮。ゾウリムシを強制的に一定周期で伸縮させると、メタクロナール波の発生周期が伸縮周期に引込まれる。
■研究概要 調和や規則性を自発的に生み出すことは生物の大きな特徴の一つです。私たちは、細胞運動のさまざまなパラメータを計測したり、細胞運動に人為的な制御を加えたときの細胞骨格の振舞いや運動の変化を光学顕微鏡で観察することで、そのメカニズムを明らかにしようとしています。例えば、ゾウリムシの両端をピペットで吸引固定し人為的に一定周期で伸縮させると(図3)、やがて繊毛のメタクロナール波の発生周期は伸縮周期と等しくなります。これはメタクロナール波の伝播するメカニズムを細胞の表層の伸縮性が担っていることを示しています。
■科学的・社会的意義 私たちの目標は、生物の大きな特徴の一つである調和や規則性の成り立ちを細胞運動を題材に解明することです。生物だからこそできるこうした現象の秘密に少しでも迫りたいと考えています。私たちの研究によって細胞運動のメカニズムの巧妙さが少しでも明らかになれば、細胞運動を模した機械の開発など独創的な工学応用に発展するかもしれません。
■参考文献
1)Nakata, T., et al. (2016). The role of stress fibers in the shape determination mechanism of fish keratocytes. Biophys J 110: 481-492.
2)Narematsu, N., et al. (2015). Ciliary metachronal wave propagation on the compliant surface of Paramecium cells. Cytoskeleton 72: 633-646.
■よく使用する材料・機器
1)倒立顕微鏡システムTi-E(株式会社ニコン)
2)共焦点ユニットCSU-X1(横河電機株式会社)
3)CCDカメラ iXon DU-897(アンドール・テクノロジーLtd)
4)光学部品(シグマ光機株式会社)
 H28年度分野別専門員
H28年度分野別専門員
山口大学大学院・創成科学研究科
岩楯好昭(いわだてよしあき)
https://biophysics.sci.yamaguchi-u.ac.jp/
「最小微生物、マイコプラズマの滑走運動」
■背景 ヒト肺炎の病原菌としても知られるマイコプラズマは、最も小さなゲノムと細胞で知られています。そのため一般的には、「マイコプラズマは栄養の豊富な培地で増殖することしかできない」と考えられています。ところが実際は、寄生のための数々の必殺技を編み出してきた強者です。マイコプラズマは、宿主の組織など固形物の表面にはりつき、はりついたままに滑るように動く“滑走運動”をします(図1、2)。運動性を持つバクテリアの多くは、“べん毛”という尻尾を回転させることで遊泳します。また、ヒト、植物、アメーバなどを含む真核生物は、筋肉と共通の仕組みで動きます。ところがマイコプラズマの滑走運動はそのどちらとも根本的に異なります。
■研究概要 日本生物物理学会では、このユニークな運動メカニズムに世界に先駆けて取り組み、最速種のマイコプラズマ・モービレについて以下を明らかにしました。すなわち、滑走装置(図3)の表面に約50ナノメートルほどの柔らかい“あし”が多数生えています。滑走装置内部でATPが加水分解されると動きが生じ、その動きが細胞膜を超えて“あし”に伝わります。“あし”は宿主表面の構造である、シアル酸オリゴ糖をつかんだり、ひっぱったり、離したりして、菌体を前に進めるのです。シアル酸オリゴ糖は、インフルエンザウイルスなどの標的としても知られています。さらに興味深いことに、最近、この装置でATPを加水分解しているタンパク質が、ほとんどの生物に存在してATPを合成している"F1-ATPase"から進化している可能性が示唆されました。
■科学的・社会的意義 これまでの生体運動分野では、ミオシンなどのモータータンパク質と、バクテリアべん毛モーターがよく調べられてきましたが、それ以外のものはあまり詳しく調べられて来ませんでした。本研究の様に、全く新しい生体運動メカニズムを理解することは、タンパク質の機能や、生物の生き残り戦略を理解するうえで重要です。また、滑走運動はマイコプラズマの寄生性に必須ですから、マイコプラズマ疾患の予防や治療にもつながります。
■参考文献
宮田真人 (2010)
病原細菌,マイコプラズマのユニークな滑走運動. 化学と生物, 48, 176-181.
https://www.sci.osaka-cu.ac.jp/~miyata/dl/history/2010ChemBiol.pdf
宮田真人(2009)
マイコプラズマ滑走運動の装置とメカニズム. 顕微鏡, 44, 210-214.
https://www.microscopy.or.jp/magazine/44_3/pdf/44-3-210.pdf
■良く使用する材料・機器
1. 質量分析器 autoflex speed(ブルカー・ダルトニクス株式会社)
2. 電子顕微鏡 JEM1010(日本電子株式会社)
3. 凍結割断装置 JFDV(日本電子株式会社)
4. 光学顕微鏡 IX-83(オリンパス株式会社)
5. EMCCDカメラ(アンドール・テクノロジーPLC)
6. クロマトグラフィーシステム AKTA pure(GEヘルスケア・ジャパン株式会社 ライフサイエンス統括本部)
7. 高速HPLCシステム 1200 Series(アジレント・テクノロジー株式会社 )
8. 表面プラズモン共鳴測定装置Biacore-X(GEヘルスケア・ジャパン株式会社 ライフサイエンス統括本部)

図1 私たちが構築しつつあるビデオアーカイブ。マイコプラズマの滑走運動や様々な生体運動が閲覧できる。“運動マシナリー”と“ビデオ”で検索のこと。
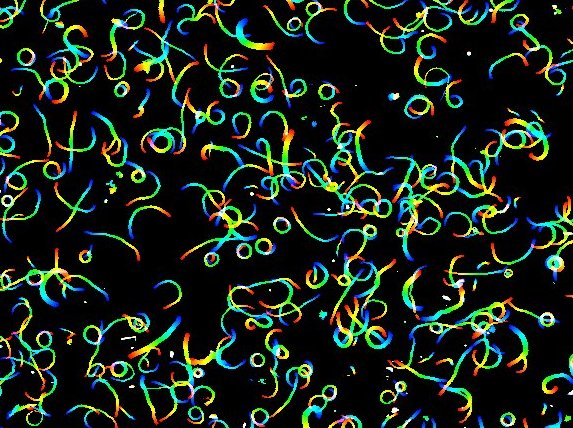
図2 マイコプラズマ・モービレの6秒間における運動軌跡。

図3 マイコプラズマ・モービレの模式図。矢印の方向へ滑走する。ピンク部分が滑走装置。
 H26年度分野別専門委員
H26年度分野別専門委員
大阪市立大学大学院理学研究科
宮田真人 (みやたまこと)
https://www.sci.osaka-cu.ac.jp/~miyata/index.html
