受容体
「代謝型グルタミン酸受容体の機能調節メカニズム」
■背景
細胞膜で働く受容体タンパク質は、細胞外の様々な情報を受けて、その情報を細胞の内側へと伝えます。膜受容体は構造と機能に応じて、Gタンパク質共役型受容体(GPCR)・イオンチャネル連結型受容体・酵素連結型受容体などに分類されています。
GPCRは刺激を受けて細胞内の3量体Gタンパク質を活性化することで、cAMP・Ca2+濃度の増減など、いくつかの細胞応答を引き起こします。ヒトは約800種のGPCRを持っており、光・匂い・味などの感覚受容を担うほか、神経伝達物質やホルモンを受けとることで、細胞間・臓器間のコミュニケーションを司ります(1)。また、GPCRは薬の標的分子としても主要な位置を占めており、現時点で約30%の低分子薬がなんらかのGPCRをターゲットとしています。したがって、GPCRがどのようにしてリガンドを受容し、その情報を細胞内へ伝えるのかを調べることは薬理学・創薬にとって重要な課題と言えます。
GPCRは細胞膜をαヘリックスが7回貫通するという共通の構造モチーフを持ちます。最初にX線結晶構造解析により原子レベルで不活性・活性状態の構造が明らかになったGPCRは、我々の視覚を担うロドプシンという光受容体でした。ロドプシンは光を吸収するためにビタミンAの誘導体である11-cisレチナールを膜貫通領域中にあらかじめ結合しています。ロドプシン中の11-cisレチナールが、光エネルギーによりall-trans型に異性化することで、膜貫通へリックスの細胞質側が閉じた構造から開いた構造へと変化します(図1)。これにより不活性状態では隠れていたGタンパク質との相互作用部位が露わになり、Gタンパク質を活性化できるようになります。近年では、様々なGPCRにおいてX線結晶構造解析や極低温電子顕微鏡解析が盛んに行われ、各種リガンドを結合した状態のGPCRの構造が200種以上報告されています(GPCRdb: https://gpcrdb.org/)。
ロドプシンやアドレナリン受容体を含む多くのGPCRは単量体でGタンパク質を活性化できますが、GPCRが生細胞膜上で二量体・多量体を形成してより高度な機能調節をする事例も数多く報告されてきました(2)。しかしながら、上述の単量体内部の構造変化に比べ、二量体・多量体化を介した機能調節メカニズムは明らかでありません。X線結晶構造解析では、特定の構造状態について空間分解能の高いスナップショットを撮影できますが、構造状態の多様性や複数の状態間の時間変化を動的に捉えることは難しいという不得意な側面もあります。また、界面活性剤を用いて細胞膜から抽出・精製した受容体タンパク質を用いるため、実際に細胞膜上でどのような高次構造を形成しているのかについては別の方法を用いた解析が必要となります。以下では、ホモ二量体化が機能に必須であることが知られている代謝型グルタミン酸受容体(mGluR)をモデルとした、GPCRの二量体・多量体化の研究例をご紹介します。
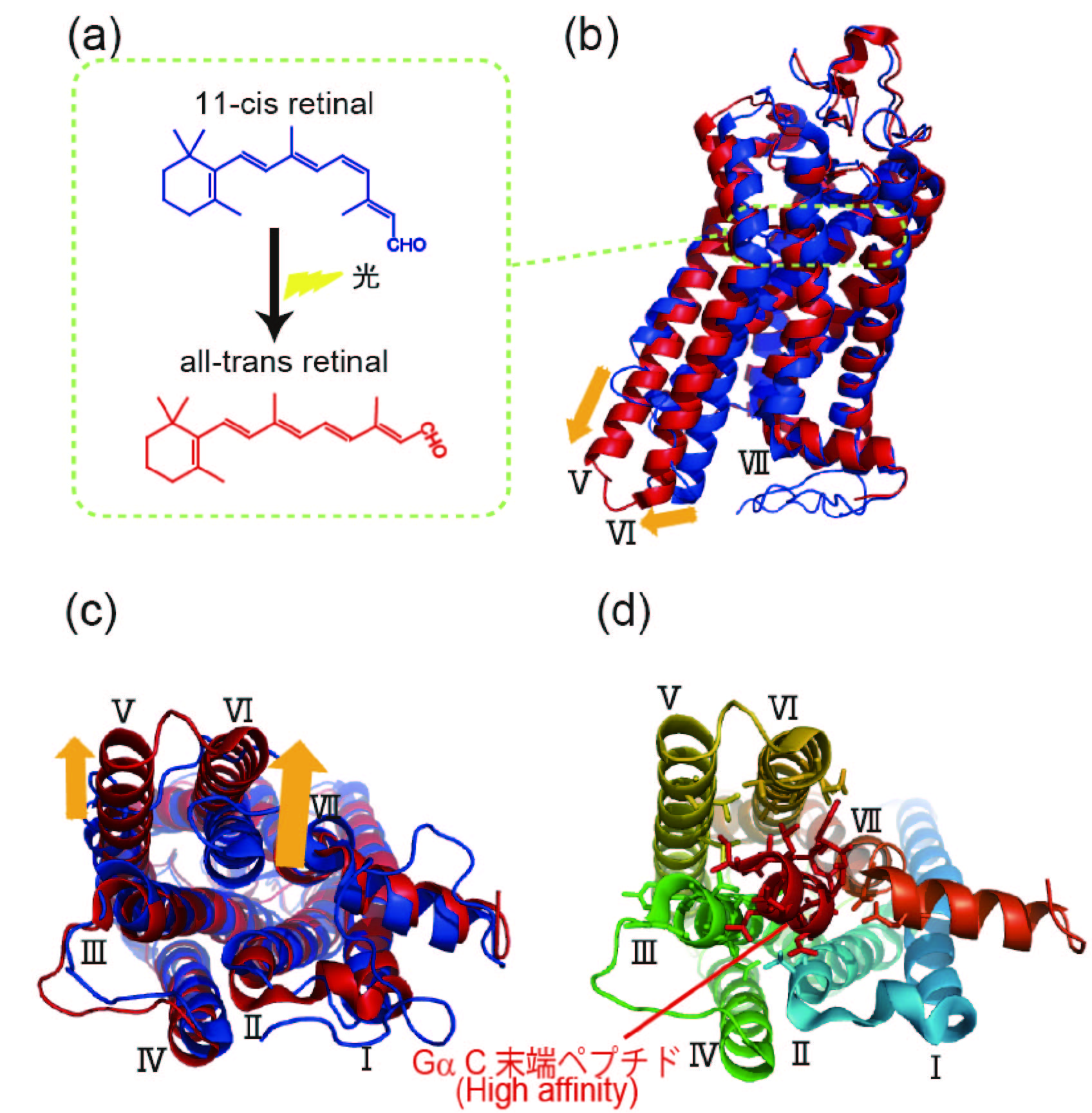
図1 ロドプシンを例とした活性化に伴うGPCRの構造変化
(a) ウシロドプシンが光を受容した時に生じるレチナールのcis-trans異性化。(b,c)ウシロドプシンの不活性(青:1U19)・活性状態(赤:3PQR)のX線結晶構造を重ね、脂質二重膜側(b)、細胞質側(c)からそれぞれ見た図。光受容に伴いヘリックスⅤが細胞質側に伸長し、ヘリックスⅥがヘリックスⅢに対して外側に広がることでGタンパク質の結合部位が露出する。 (d) Gタンパク質のαサブユニットのC末端ペプチドと活性化ウシロドプシンの相互作用(3PQR)。
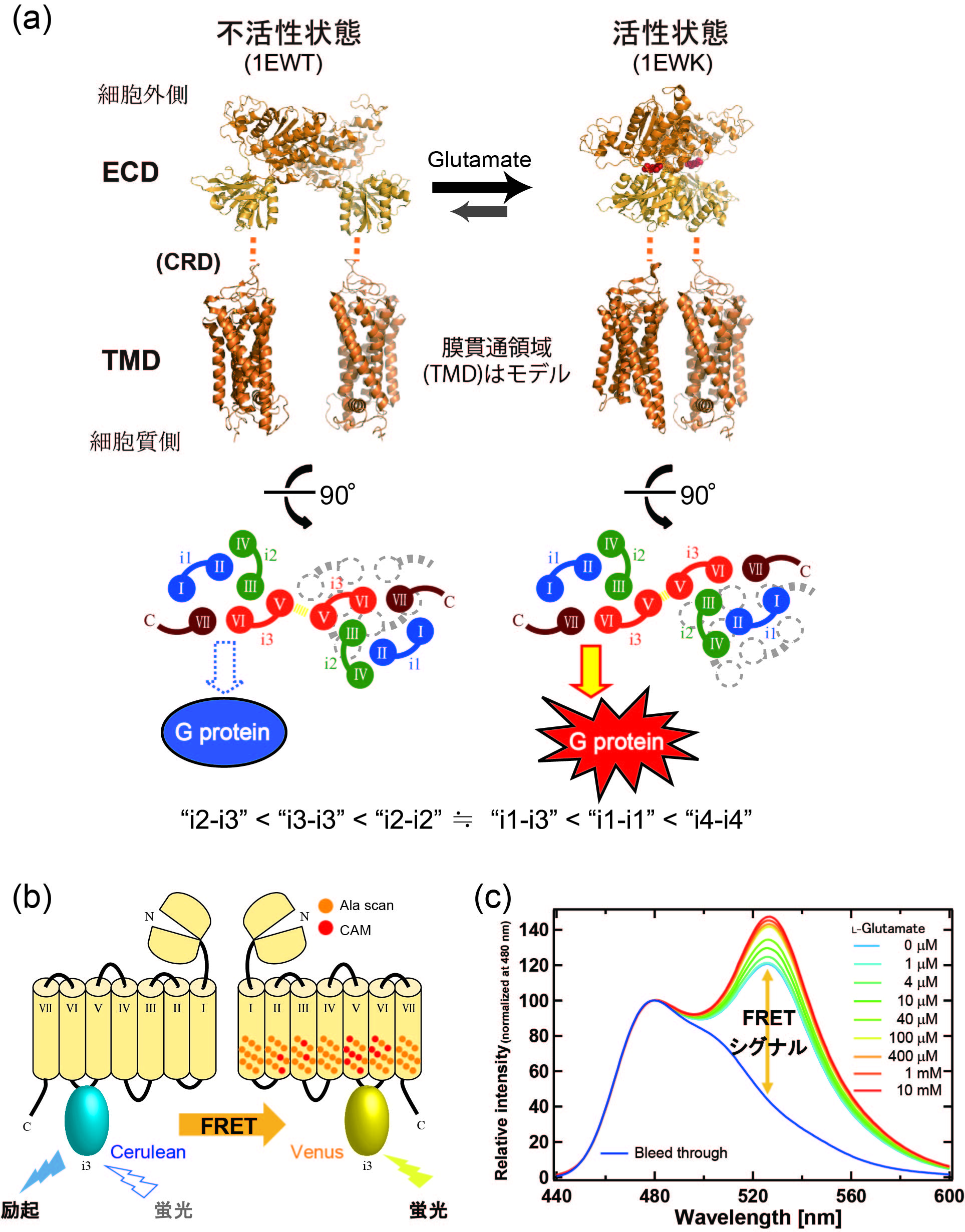
図2 FRET解析から推定される代謝型グルタミン酸受容体の二量体配置転換
(a) mGluRの活性化機構のモデル。細胞外領域(ECD)の不活性状態(1EWT)・活性状態(1EWK)のX線結晶構造の細胞質側に、FRET解析から推定された二量体配置に膜貫通領域(TMD)のモデルを置いた。図下の不等式はFRET効率の大小から推定される各細胞質ループ領域i1, i2, i3, i4(C末端) 間の距離関係。(b) mGluRに融合した蛍光タンパク質Cerulean-Venus間に生じるFRETの模式図。Ceruleanを励起した際に、蛍光タンパク質間の距離に依存してFRETが生じ、Ceruleanからの蛍光が低下するとともに、Venusの蛍光が上昇する。網羅的なアラニンスキャン変異体解析の結果、構成的活性化変異(CAM)が同定されたアミノ酸残基の位置をmGluRの模式図の右側のサブユニットに赤丸で示した。(c)分光蛍光光度計を用いて433nmの励起光下で計測した、Cerulean-Venus融合mGluRの蛍光スペクトル例。グルタミン酸濃度依存的にVenus由来の蛍光強度比が増加し、FRET効率が上昇することが示された。
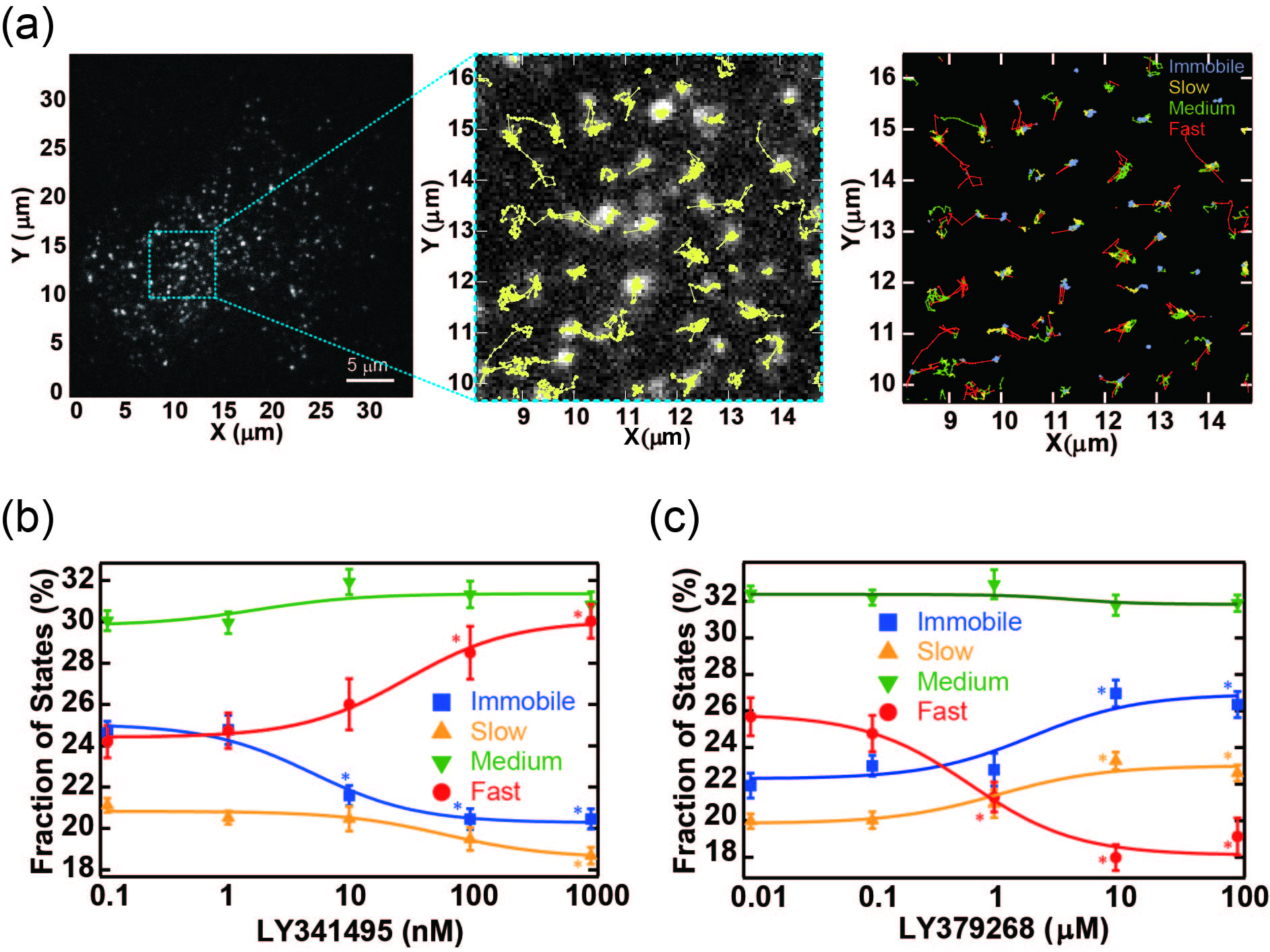
図3 1分子イメージングによるmGluRのリガンド依存的な拡散動態変化
(a) mGluRの1分子イメージ例。1つのHEK293細胞の形質膜に局在するmGluRの分子を輝点として観察できる。中央パネルは左パネルの青点線を拡大した図。黄線は、各mGluRの輝点の軌跡。右パネルは隠れマルコフモデルを用いて、中央パネルの軌跡を4つの拡散状態(青: Immobile, 黄:Slow, 緑:Medium, 赤:Fast)に分類した例。(b,c) リガンド依存的なmGluRの拡散状態の割合の変化。(b) mGluRを不活性化するインバースアゴニスト濃度依存的にFastの割合が上昇し、Immobileの割合が低下する。(c) mGluRを活性化するアゴニスト依存的にFastの割合が低下し、Slow・Immobileの割合が上昇する。
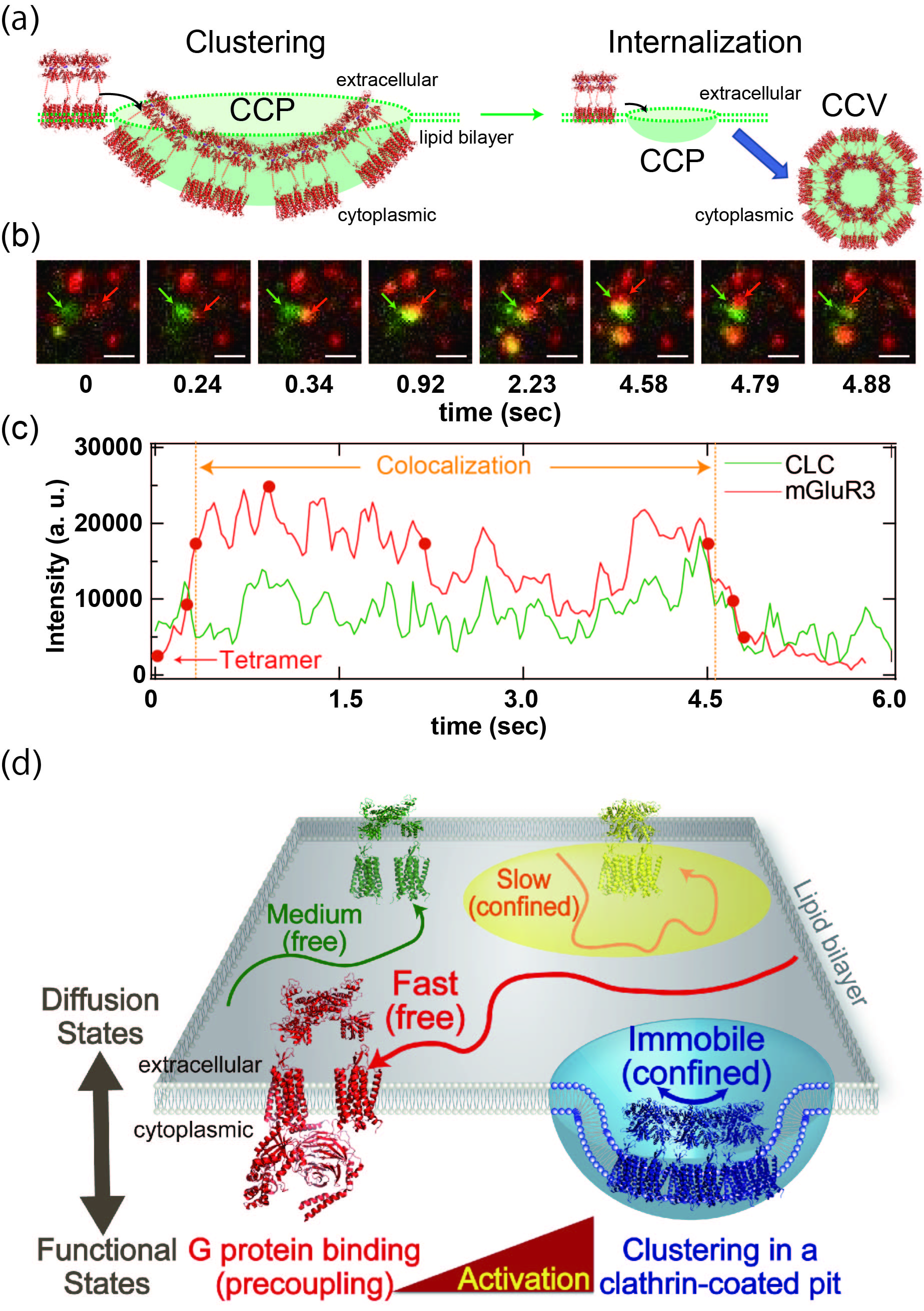
図4 2色同時1分子イメージングによるmGluRのクラスリン被覆ピットへの集積の観察
(a) mGluRがクラスリン被覆ピットに集積した後、クラスリン被覆小胞が細胞膜内へと輸送される過程の模式図 (b) mGluR(赤)とクラスリン軽鎖(緑)の2色同時一分子計測例。0.34秒で2色の輝点が共局在した後、mGluRの輝点が同領域に集積し、4.5秒で両輝点が同時に暗くなって細胞膜上から消える。 (c) (b)に示した両輝点の時系列変化。(d)1分子イメージング解析から推定されるmGluRの拡散状態と機能状態の対応関係の模式図。
■研究概要
代謝型グルタミン酸受容体の活性化メカニズム
mGluRは我々の脳神経系に広く局在しており、主要な神経伝達物質であるグルタミン酸を受容し、神経細胞間の情報伝達を担います。mGluRは細胞外に大きなリガンド結合領域を持っており、2つの細胞外領域が共有結合によってつながれて常に二量体として機能します(図2a)。これまでの研究からグルタミン酸の結合が引き起こす細胞外領域の二量体の配向変化がmGluRの活性化に重要であると考えられてきましたが、細胞外領域の構造変化がどのようにして膜貫通領域に伝わるのかは不明でした。特に、グルタミン酸結合がmGluRの膜貫通領域にどのような二量体の配置転換を引き起こすのかを知ることは、GPCRの二量体化による機能調節メカニズムを解明する上でも重要です。
そこで我々は、mGluRを2色の蛍光タンパク質で標識し、蛍光色素間に生じる蛍光共鳴エネルギー移動(FRET)を分光蛍光光度計により定量することで、細胞膜画分中のmGluRの膜貫通領域の二量体配置を推定しました(3) (図2b, c)。FRET計測では2つの蛍光色素が近接して存在する時、色素間に生じるエネルギー移動の効率(FRET効率)を定量します。FRET効率は2つの蛍光色素間距離に依存して変化するため、2色の蛍光色素でタンパク質をラベルすれば、ラベル間の距離を測る「ものさし」として利用することができます。
GPCRは7本の膜貫通へリックスをつなぐ3つの細胞質ループ領域とC末端領域を細胞質側に持ちます。本研究では、mGluRの上記の4つの細胞質領域をCerulean(青色)・Venus(黄色)の2色の蛍光タンパク質でそれぞれラベルをした融合タンパク質を作成し、それらを網羅的に組み合わせて、各領域間の距離関係をFRET効率から推定しました(図2b-c)。その結果、ヘリックスV-VIをつなぐ細胞質第3ループ間の距離が最も近接して存在することが示唆されました。さらに、グルタミン酸濃度依存的にFRET効率の上昇が生じたことから、mGluRの活性化に伴い2つの膜貫通領域が互いに近づくことが明らかになりました(図2a)。
さらに我々は、膜貫通領域のどのようなアミノ酸残基がmGluRの活性化に重要なのかを調べるために、7本の膜貫通へリックスを構成する各アミノ酸残基をアラニンに置換する網羅的な変異体解析を行いました(4,5)。その結果、FRET解析から二量体のインターフェースを形成すると予想されたヘリックスV-VIの細胞質側に変異を入れると、グルタミン酸が結合していない状態でもGタンパク質を活性化する変異体がたくさん見つかりました(図2b)。したがって、これらのアミノ酸残基がmGluRの膜貫通領域を不活性状態に維持する上で重要なアミノ酸残基間相互作用を担うことが示されました。
以上の研究結果を総合することで、次のようなmGluRの活性化メカニズムが推定されました。まず、mGluRがグルタミン酸を受容すると、細胞外リガンド結合領域の二量体の配向が変化します。この細胞外領域の配向変化は、細胞外領域と膜貫通領域をつなぐリンカー領域を介して膜貫通領域へと伝わり、2つの膜貫通領域が互いに近づきます。この際、二量体のインターフェースが変化することで、それぞれの膜貫通領域内部のアミノ酸残基間相互作用がスイッチし、Gタンパク質を活性化する領域が細胞質側へと提示されると考えられます。mGluRは上述のロドプシンとはアミノ酸配列の相同性がほとんどなく、膜貫通領域の構造変化を引き起こす原動力も異なりますが、最終的にヘリックスV-VIの細胞質側の構造変化が活性化に重要であるという点で機能調節メカニズムを共有しているのかもしれません。
生細胞における代謝型グルタミン酸受容体の拡散動態変化と高次多量体形成
さらに、我々はより生体に近い環境でmGluRがどのように活動しているかを調べるため、生きた細胞においてmGluRの1分子イメージングを行ってきました。全反射蛍光顕微鏡を用いることで、カバーガラス上に培養した細胞の底面から約200nmの領域を励起して観察することができます。これにより細胞内に局在している蛍光色素由来のバックグラウンドが低減され、受容体の発現量が低い細胞では、細胞膜に局在する個々の受容体分子を輝点として捉えることができます(6)。
我々は、ヒト胎児腎細胞由来のHEK293細胞にmGluRを発現し、C末端領域を蛍光色素で標識して全反射蛍光顕微鏡計測を行いました(7) (図3)。撮影した動画の各mGluR分子の輝点を追跡して軌跡を解析することで、受容体の拡散動態を定量することができます。また、蛍光色素1分子あたりの明るさから、mGluRの多量体サイズを推定することが可能です。様々なリガンド条件下で1分子計測を行い、拡散係数の平均値を比較したところ、mGluRの活性と相関して拡散係数が変化することが明らかになりました。活性化したmGluRは拡散が遅くなるとともに、4量体以上の高次多量体を形成します。さらに、2色同時1分子イメージングによりmGluRとクラスリンの共局在を調べたところ、mGluRが活性化に伴って集積して動かなくなる細胞膜領域のひとつがクラスリン被覆ピットであることが分かり、mGluRの拡散がリガンド依存的に変化した背景が明らかになりました(図4)。
GPCRは活性化するとGタンパク質と相互作用するとともに、GRKによってC末端部位をリン酸化されます。このリン酸化部位を認識してアレスチンが結合することで、GPCRはGタンパク質と相互作用できなくなります。GPCRと結合したアレスチンは様々なタンパク質と相互作用することが知られていますが、その代表的な分子がクラスリンです。クラスリンが細胞膜上で重合して形成されるクラスリン被覆ピットは、GPCRを細胞内へと輸送し、リサイクル・分解する一般的な機構を担うことが知られています。このため、活性化に伴い拡散が遅くなるという現象はmGluRだけでなく、様々なGPCRに共通しているのではないかと推測されました。実際に、mGluRとはホモロジーがほとんどなく、活性化するGタンパク質の種類も様々な8種のGPCRについても同様の1分子イメージングを行ったところ、リガンド刺激依存的に拡散が遅くなることが共通して確認されました。
本研究で明らかになったGPCRの機能状態と拡散係数の相関関係を利用することで、GPCR自体の動きを見てリガンドの薬効を評価がすることができると期待されます。
■科学的・社会的意義
本研究では、mGluRをモデルとしてGPCRの二量体配置転換による機能調節メカニズムを明らかにしてきました。GPCRの二量体は副作用の少ない新たな薬のターゲットとして注目されていますが、どのように二量体のインターフェースを安定化すれば、どのような薬効を生むかはほとんど分かっていません。本研究の成果は、その一端を明らかにしたという点で薬理学的に重要です。
また、本研究により、9種のGPCRに共通してリガンド依存的に拡散係数が変化することがはじめて分かりました。GPCRの拡散係数は、リガンド・シグナル伝達経路が未知のオーファン受容体であっても蛍光標識をすれば全反射顕微鏡計測により定量することができます。したがって、本研究成果を応用して、1分子イメージングを用いたGPCRのリガンドスクリーニングシステムを構築すれば、創薬に新たな手法を提供できると期待されます。
■参考文献
1)柳川, 七田. (2013). 「Gタンパク質共役型受容体の進化」 生体の科学 64(4):366-74
2)柳川, 七田. (2011). 「GPCRの二量体化による機能制御メカニズム」 生化学 83(10):949-56
3)Yanagawa, M., Yamashita, T., Shichida, Y. (2011). "Comparative fluorescence resonance energy transfer analysis of metabotropic glutamate receptors: implications about the dimeric arrangement and rearrangement upon ligand bindings." J Biol Chem. 286(26):22971-81.
4)Yanagawa, M., Yamashita, T., Shichida, Y. (2009). "Activation switch in the transmembrane domain of metabotropic glutamate receptor." Mol Pharmacol. 76(1):201-7
5)Yanagawa, M., Yamashita, T., Shichida, Y. (2013). "Glutamate acts as a partial inverse agonist to metabotropic glutamate receptor with a single amino acid mutation in the transmembrane domain." J Biol Chem. 288(14):9593-601.
6)柳川, 佐甲. (2017). 「細胞膜受容体の1分子イメージング」生体の科学 64(4):366-74
7)Yanagawa, M., Hiroshima, H., Togashi, Y., Yamashita, T., Shichida, Y., Murata, M., Ueda, M., and Sako, Y. (2017). "Single-molecule diffusion-based estimation of GPCR activity" bioRxiv. [doi: https://doi.org/10.1101/205161]
■良く使用する材料・機器
1)分光蛍光光度計 RF5300PC(株式会社島津製作所)
2)蛍光顕微鏡システム Ti-E (株式会社ニコン)
3)EM-CCDカメラ ImagEM (浜松ホトニクス株式会社)
4)蛍光色素 HaloTag ligand (プロメガ株式会社・五稜化薬株式会社)
5)実験試薬(和光純薬株式会社)
 H29年度分野別専門委員
H29年度分野別専門委員
理化学研究所・佐甲細胞情報研究室
柳川正隆 (やながわまさたか)
https://www.riken.go.jp/cell-info/
