糖・糖鎖・糖脂質
「糖鎖の多様性の不思議に物理で迫る」
■背景
糖鎖は、生体内でマンノースなどの単糖(図1A)がつながって出来上がります。DNAやタンパク質は鋳型を基に作られるため均一性が高いのですが、糖鎖は鋳型に依存しないため、一般に不揃い(不均一)です。工業製品に例えると、DNAやタンパク質は品質テストに合格しますが、糖鎖は不合格になるでしょう。しかし、生体はこの一見不良品のような糖鎖を巧みに利用しています。例えば、免疫システムで働く抗体には、図1Bに示すように不揃いな糖鎖が結合していますが、個々の糖鎖は抗体の働きを調節していることがわかっています。ABO血液型抗原の実体も糖鎖ですが、輸血時にA型とB型を間違えると、構造のわずかな違いにより、免疫システムにより異物として認識されます(図1C)。このように曖昧さと厳密さを示す糖鎖は、生体内でどのような法則に基づいて機能しているのでしょうか?糖鎖についてはわかっていないことが多く残されています。
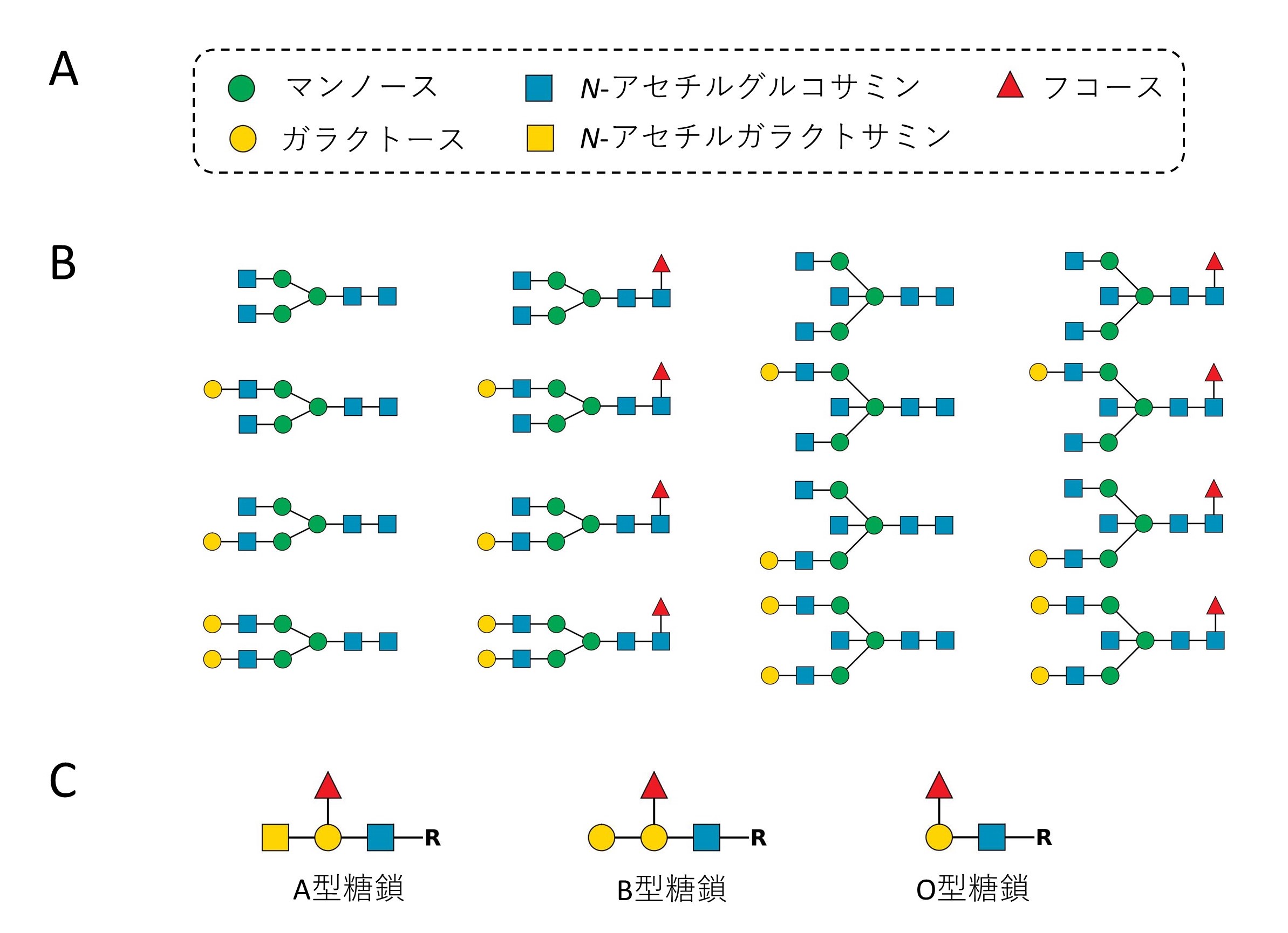
図1 多様性を示す糖鎖の例。A: 糖鎖を構成する糖(単糖)の例とそのシンボル表示。B: 抗体(タンパク質)に結合している糖鎖の不均一性の例。C: 脂質に結合しているABO血液型糖鎖抗原。AB型はA型とB型の糖鎖を両方もつ。
■研究概要
「百聞は一見に如かず」ということわざがあるように、生体分子の働きを調べるには、生体分子の形を直接“見る”ことが有効です。不揃いな糖鎖の働きを明らかにするためには、糖鎖一つ一つの形や動き、相手との相互作用の様子を“見る”ことが大事になります。一般に糖鎖は柔らかい分子であり、その形を実験的に捉えることは難しいのですが、糖鎖をタンパク質(レクチン)と結合させることにより、通常では見ることのできない折れ曲がり型の糖鎖を可視化することに成功しました(図2、文献1)。また、糖鎖は構造が似ているものの混合物であり、一つ一つの構造の同定には困難を伴いますが、糖鎖の形に着目した方法を用いることにより、よく似ている糖鎖の識別に成功しました(図3、文献2、3)。
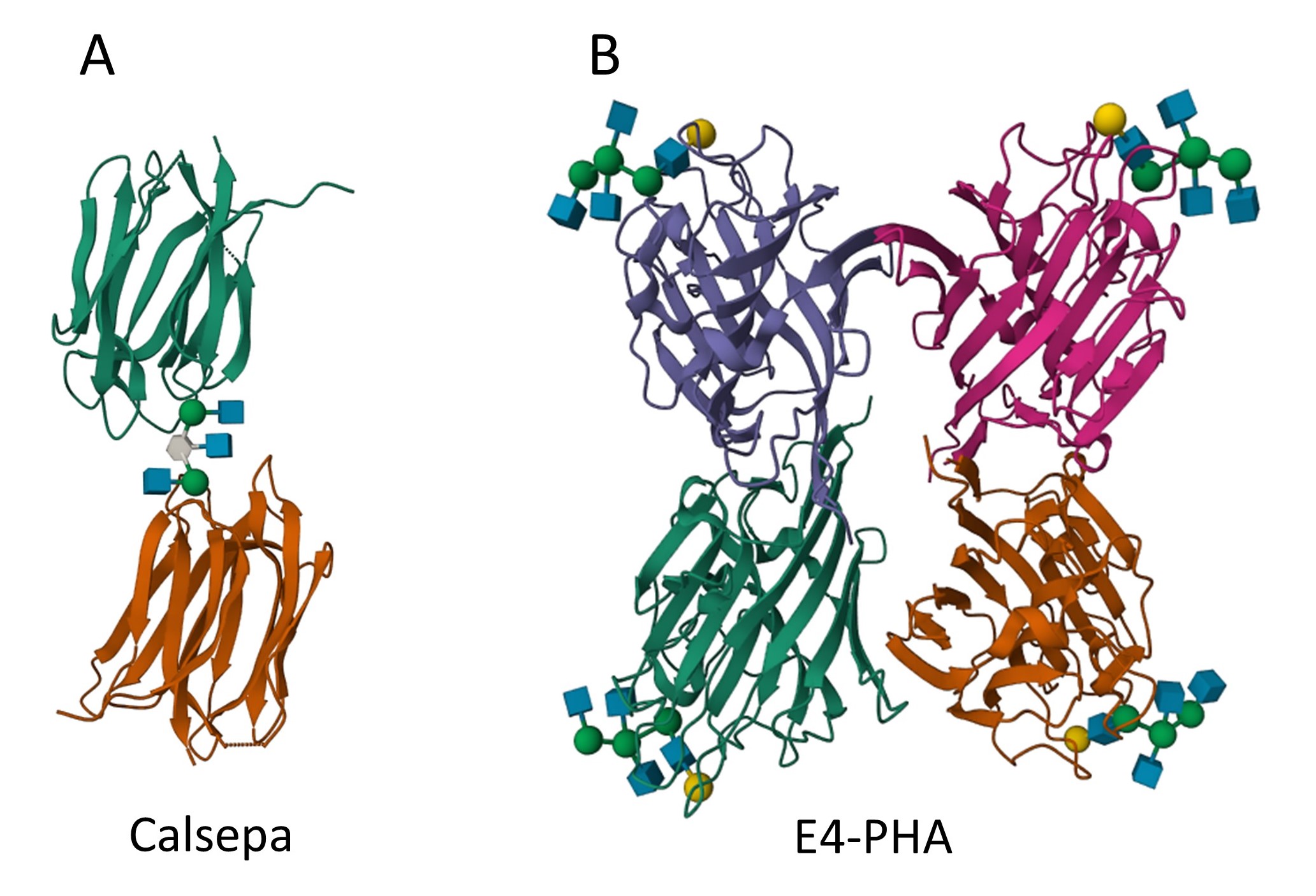
図2 柔軟な糖鎖の折れ曲がり構造の可視化。糖鎖をCalsepaレクチン(A)やE4-PHAレクチン(B)と結合させることにより、糖鎖の取り得るマイナーな構造を可視化している。糖鎖はシンボルにて表示し、タンパク質はリボンにて表示している。
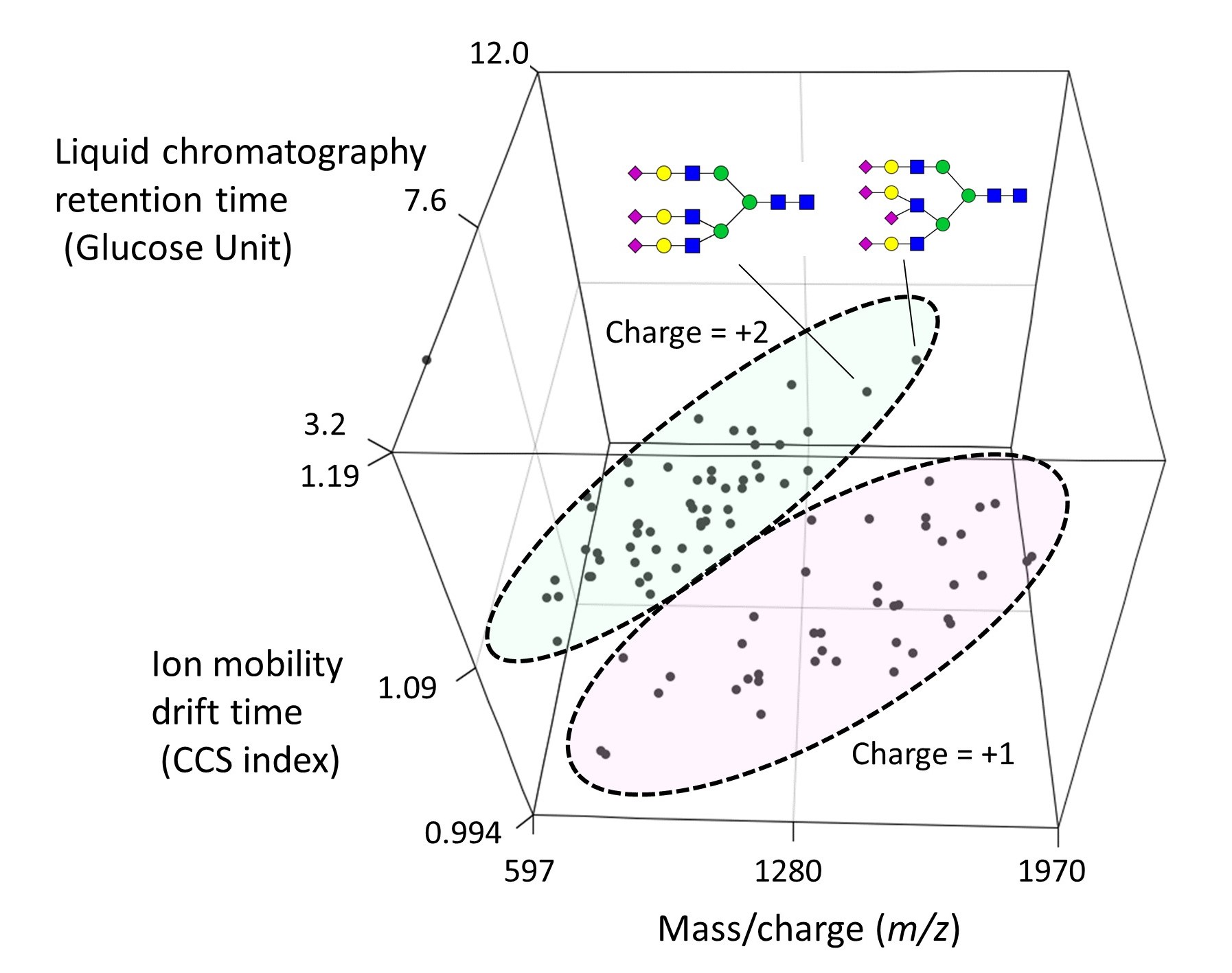
図3 イオンモビリティ質量分析法(IM-MS)と液体クロマトグラフィー(LC)による糖鎖構造解析のためのデータセット。一つ一つの点は各糖鎖に対応しており、実験結果との照合により、糖鎖の同定作業を迅速化します。
■科学的・社会的意義
本研究は、糖鎖のもつ多様性の意義の解明につながります。また、基礎研究の分野だけでなく、糖鎖の関係する病気の診断や治療など、医療の分野に貢献することも期待されています。
■参考文献
1)Nagae, M., Kanagawa, M., et al. (2016). "Atomic visualization of a flipped-back conformation of bisected glycans bound to specific lectins." Sci Rep. 6:22973.
2)Yamaguchi, Y., Nishima, W., et al. (2012). "Confident identification of isomeric N-glycan structures by combined ion mobility mass spectrometry and hydrophilic interaction liquid chromatography." Rapid Commun Mass Spectrom. 26(24):2877-84.
3)Manabe, N., Ohno, S., et al. (2022). "A data set of ion mobility collision cross sections and liquid chromatography retention times from 71 pyridylaminated N-linked oligosaccharides." J Am Soc Mass Spectrom. 33(9):1772-1783.
■良く使用する材料・機器
1) 実験試薬 (和光純薬株式会社)
2) 安定同位体標識化合物 (太陽日酸株式会社)
3) 核磁気共鳴装置 (ブルカージャパン株式会社、日本電子株式会社)
4) イオンモビリティ質量分析装置 (日本ウォーターズ株式会社)
 2023年分野別専門委員
2023年分野別専門委員
東北医科薬科大学・分子生体膜研究所
山口芳樹 (やまぐちよしき)
https://www.tohoku-mpu.ac.jp/pharmacy/lab/lp_e02/
「細胞膜分子の相互作用を1分子ごと手に取るように観察する」
■背景 生体膜は、脂質2重層に膜たんぱく質が浮かんだ2次元液体であり、受容体を介して外界と情報のやり取りの場を提供しています。近年、情報伝達の場として脂質ラフトという概念(図1)が注目されていますが、構造や役割はほとんど明らかになっていませんでした。
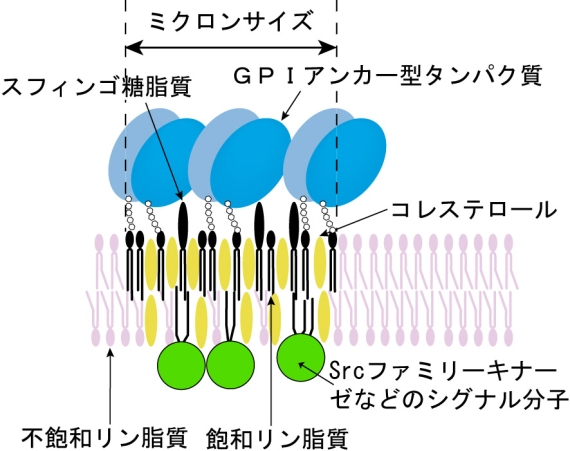
図1 提案された当初のラフトの概念図
ラフトは、ミクロンサイズと大きく、多くの分子を集めている。GPIアンカー型受容体、スフィンゴ糖脂質(ガングリオシド)、コレステロール、脂質アンカー型シグナル分子などが主な構成成分とされている。
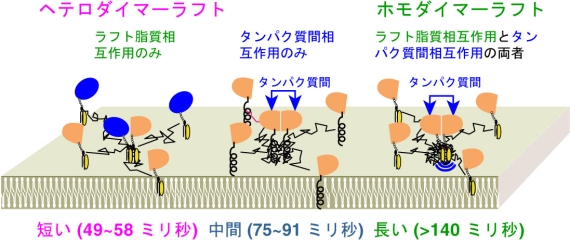
図2 GPIアンカー型受容体を含む短寿命ラフト形成
GPIアンカー型受容体のホモダイマーは、タンパク質相互作用により形成され、ラフト脂質相互作用により安定化される。
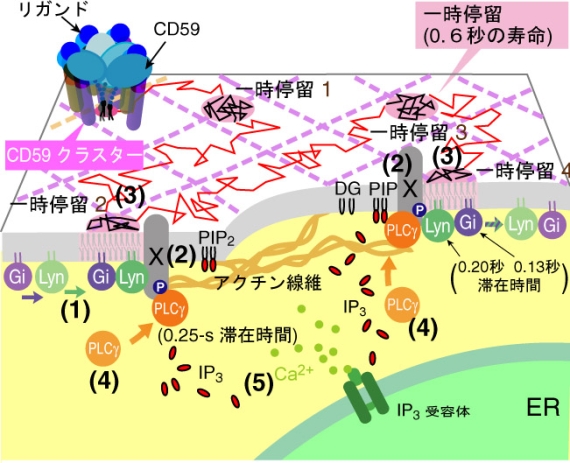
図3 CD59オリゴマーラフトによるシグナル伝達の素過程
シグナルにより受容体CD59が会合すると、安定なラフト(オリゴマーラフト)ができる。このオリゴマーラフトは膜上を動き回り、アクチン線維上で一時停留時に下流のシグナル伝達のプラットフォームとしてはたらく。
■研究概要 この疑問に答えるため、ラフトマーカーである、GPI(グリコシルホスファチジルイノシトール)アンカー型受容体や糖脂質の1分子ずつの挙動を追跡しています。これまでに定常状態において、ミクロンサイズの大きなラフトは存在せず、GPIアンカー型受容体のホモダイマーからなる非常に小さく短寿命(~200ミリ秒)のラフトが形成されていることがわかりました(図2、文献1,2)。また、受容体を刺激後には、非常に安定な受容体オリゴマーラフトがタンパク質相互作用とラフト相互作用により形成され、下流のシグナル分子を数百ミリ秒という短い期間、活性化することが判明しました(図3、文献3,4)。また、ラフト中のシグナル分子のパルス状(デイジタル式)の活性化は、細胞全体のシグナル強度を微調整(チューニング)するのに最適であると提案しています。
■科学的・社会的意義 ラフトの実態を解明することにより、ラフトが関連すると言われている疾病(アルツハイマー病やBSEなど)の発症機構の研究にも役立つと期待されます。
■参考文献
1)Suzuki, K.G.N. et al. (2012). "Transient GPI-anchored protein homodimers are units for raft organization and function" Nature Chem. Biol. 8(9): 774-783.
2)Tanaka, K.A.K* and Suzuki, K.G.N*, et al. (*equal contribution) (2010). "Membrne molecules mobile even after chemical fixation" Nature Methods 7(11): 865-866.
3)Suzuki, K.G.N. et al., (2007) “GPI-anchored receptor clusters transiently recruit Lyn and G alpha for temporary cluster immobilization and Lyn activation: single-molecule tracking study 1.” J. Cell Biol. 177(4): 717-730.
4)Suzuki, K.G.N. et al., (2007) “Dynamic recruitment of phospholipase C gamma at transiently immobilized GPI-anchored receptor clusters induces IP3-Ca2+ signaling: single-molecule tracking study 2.” J. Cell Biol. 177(4): 731-742.
■良く使用する材料・機器
1) 全反射顕微鏡システム(株式会社ニコンあるいはオリンパス)
2) EB-CCDカメラ (浜松ホトニクス株式会社)
3)ハイスピードカメラ(株式会社フォトロン)
 H24年度分野別専門委員
H24年度分野別専門委員
京都大学・物質-細胞統合システム拠点
鈴木健一(すずきけんいち)
https://www.nig.icems.kyoto-u.ac.jp/suzuki-j/homu.html
