ミトコンドリア
「細胞内に張り巡らされたエネルギープラント」
■背景
私たちヒトをはじめとした真核生物は、多数の細胞が集まることで組織・器官を形成し成り立っている(多細胞生物)。その最小単位である細胞(真核細胞)は、核を中心に小胞体やゴルジ体、さらにはミトコンドリアなどのさまざまな細胞小器官(オルガネラ)が独自の機能を発揮して、それぞれに細胞の営みに関わっている。なかでもミトコンドリア(図1)は、その特有の構造および機能からユニークなオルガネラとして今日に至るまで多くの研究者の実験材料として用いられてきた。
ミトコンドリアはその起源として、プロテオバクテリアのような好気性細菌が真核細胞の前身となる細胞に寄生することで、その後の共生進化を経て現在のような形に落ち着いたと考えられている(リン・マーギュリスによる細胞内共生説;1967年)。例えば、ミトコンドリア内には核とは独立したゲノム(ミトコンドリアDNAと呼ぶ)が存在し、また他のオルガネラには見られない二重の膜構造になっていることなどは、このオルガネラが細胞本体以外の別の生物に由来すること連想させる。
細胞内におけるミトコンドリアの重要な役割としては、エネルギー(アデノシン三リン酸;ATP)の産生である。それ以外にも、細胞内カルシウムイオン濃度の調節や脂質の酸化、また近年は免疫反応においても不可欠な働きをしていることが明らかになってきた。このように、ミトコンドリアは細胞の営みにおいて、まさに司令塔のような役割をしており、更なる役割を解き明かすために現在でも世界中で盛んに研究が行われている。
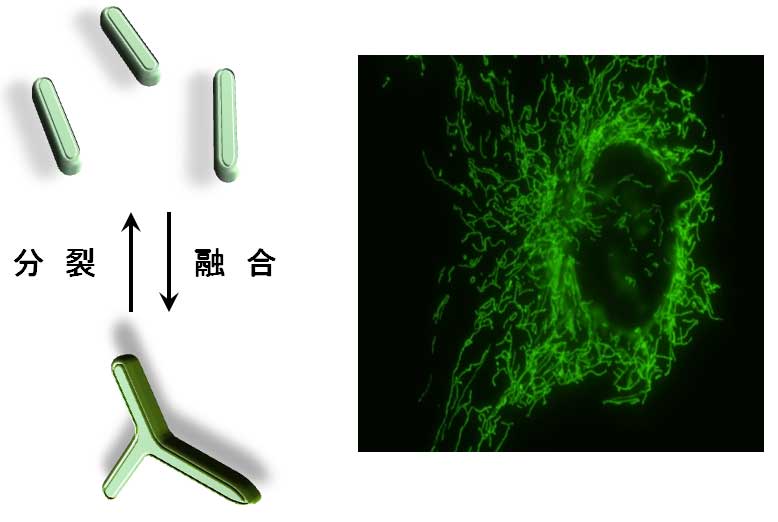
図1 細胞内のエネルギープラント:ミトコンドリア。
右写真;マウス繊維芽細胞内でのミトコンドリアの様子を光学顕微鏡で観察した。緑色に見えるひも状のものが全てミトコンドリアである。中心部の黒く見える一帯は核。
右図;ミトコンドリアは細胞内で活発に融合と分裂を繰り返している。
■ユニークな形をしたミトコンドリア
私たちが教科書などでミトコンドリアを勉強する際に、その形態をピーナッツ状の構造物(大きさ~10μm)として描写された図を一般によく目にする。しかしながら、実際に生きた細胞内におけるミトコンドリアの形は非常にユニークで、細胞質全体に管状の網様構造(tubular network)を形成・分布し (図1;写真)、絶えず融合と分裂を繰り返す運動性に富んだオルガネラと言える。このようなダイナミックな形は、全てが核にコードされた十数種類のタンパク質群によって調節されている。興味深いことに、ミトコンドリア自身の形を調節するために、ミトコンドリアDNA由来のタンパク質は関与していない。これら形態を調節するタンパク質は主に酵素であり、共通してグアノシン三リン酸(GTP) 結合タンパク質(GTPase)である。それらGTPaseの働きにより、ミトコンドリアの融合や分裂、また輸送などの動的な過程を制御している。現在でもその詳細な分子メカニズムは分かっていないが、おそらくGTPの加水分解時に放出される高エネルギーを利用してこのようなミトコンドリア・ダイナミクスを支えていると考えられている。
ところで、細胞内のミトコンドリア・ダイナミクスは真核生物にとってどのような生理的な意味があるのだろうか? この疑問に対して、残念ながら私たちは明確な回答を持ち合せていないが、モデル動物を使った研究によって明らかになってきたことがある。例えば、発生過程やシナプスの形成、さらには免疫反応においてもミトコンドリア・ダイナミクスは重要であることが次第に明らかになってきている。
■科学的・社会的意義 ミトコンドリア・ダイナミクスの破綻は、ヒトの疾患とも密接に関係していることが報告されてきた。今後の研究により、その調節メカニズムに関するタンパク質群の役割と、動物実験を中心とした個体レベルでの生理機能解析が互いに補完すれば、関連するミトコンドリア疾患の予防や、将来的には創薬探索などにおける有効な実験系の確立に期待ができる。
■参考文献
1)Yoshizumi, T. et al. (2017) RLR-mediated antiviral innate immunity requires oxidative phosphorylation activity. Sci. Rep., 7, 5379.
2)Yoshizumi, T. et al. (2014) Influenza A viral protein PB1-F2 translocates into mitochondria via Tom40 channels and impairs innate immunity. Nat. Commun., 5, 4713.
3)Koshiba, T. et al. (2011) Mitochondrial membrane potential is required for MAVS-mediated antiviral signaling. Sci. Signal., 4, ra7.
4)Yasukawa, K. et al. (2009) Mitofusin 2 inhibits mitochondrial antiviral signaling. Sci. Signal., 2, ra47.
5)Koshiba, T. et al. (2004) Structural basis of mitochondrial tethering by mitofusin complexes. Science, 305, 858-862.
■良く使用する材料・機器
1) 共焦点レーザー顕微鏡システム ECLIPSE Ti2 (株式会社ニコン)
2) 実験試薬 (和光純薬株式会社、同仁化学研究所)
3) 抗体(アブカム、CSTジャパン株式会社)
 H29年度分野別専門委員
H29年度分野別専門委員
九州大学・理学部生物学科
小柴 琢己 (こしば たくみ)
https://www.biology.kyushu-u.ac.jp/~koshiba/
