分子集合
「分子集合の基本原理」
■背景
かたちあるものは、生物・非生物にかかわらず、全て分子が集まってできています。もっと言えば、分子は原子が集まって、原子は素粒子が集まってできたものですが、化学や生物の分野では、素粒子同士の結合や原子同士の共有結合は除いて、イオン結合、ファンデルワールス力、水素結合といった、分子間に働く比較的弱い力による集合を扱うことが通例です。また、これに、疎水性相互作用や枯渇力といった、聞きなれない結合力も加わります(これらについては後述します)。
なぜ弱い力が重要かというと、私たちが日常的に経験するような、比較的マイルドな温度や圧力、エネルギーの変化やゆらぎで、分子同士が結合したり離れたりするからです(このことを正しく理解するためには、気軽に使われる「力」や「エネルギー」の定義を正しく理解する必要があります。分子結合においても、重力と分子間力を入れ替えれば、物理Iで習った重力と位置エネルギーの関係が成り立つことを意識してください)。共有結合の変化は、空気中で紙が燃えるような大きなエネルギーの投入や放出を伴いますが、私たちの身体はそこまで高温にはなりませんね。身体の中では共有結合が変化する反応も起こってはいますが、弱い力による分子同士の結合の変化も多く起こっていて、それによって私たちはほぼ一定の温度環境下でも反応したり動いたりできます。分子レベルにおいて、その集合状態が常に変化しているのです。
分子集合が関係する現象は無数にあるので、この紹介記事ではその全てを紹介することはとてもできません(1冊の本でも紹介しきれません)。ここでは、いくつかの例を挙げ、次に私が研究している脂質分子の集合を少し詳しく紹介するにとどめたいと思います。
まず、生物物理の分野で最も精力的に研究されているタンパク質は、アミノ酸が並んだひも状の分子が様々な分子間力によりある一定の形に折りたたまります(B-02, B-11, B-14, B-15, B-17, B-18, B-19を参照)。また、これらの折れたたまったタンパク質同士が、さらに結合サイトのパターンや形状に応じて会合し、巨大な複合体を形成することでより複雑な機能を持つことができます。DNAも、4種類の塩基の並びの相補性から特定配列の一本鎖DNAだけが正確に結合します。塩基配列を人工的にデザインした複数の一本鎖DNAを同じ溶液中に入れると、特定の配置で組み上がり、タイルや立方体、ひいてはスマイルマークなどのナノ構造ができます(文献1)。この技術を、DNAオリガミと呼びます。
■研究概要
上述のように分子集合は非常に広い概念ですが、ここでは、私が研究を続けている、脂質分子の分子集合に関して簡単に述べます。
リン脂質は、身近にある石けんの分子と同様に、親水性の部分と疎水性の部分を併せ持つ分子です。このような性質を持つ分子は、両親媒分子と呼ばれます。リン脂質は、水中では疎水性の部分は水を避けるので、疎水性の部分同士が寄り合って、親水性の部分が水側を向き、脂質二重層と呼ばれる膜構造をつくります。これが、細胞を包む細胞膜、ミトコンドリアなど細胞小器官を包む膜、そして特定の分子を包む数十ナノメートルの小胞といった、様々なスケールでの万能界面として使われています(A-19, A-20, B-07, B-08も参照)。通常、細胞では親の細胞が分裂して子孫ができますが、そのときには、細胞内で合成された新しい脂質分子が既存の脂質分子に足され、膜面積が増えていき、ある時点で中央付近がくびれて分裂します。つまり、もともとあった膜に膜を構成する分子が足されて、膜が増えていきます。しかし、脂質膜はもっと人工的な方法で簡単につくることができます。生物から抽出した、または化学合成したリン脂質を乾燥させてフィルム状にしたものに水を加えると、リン脂質が膜構造を保ったまま水和して膨れ上がり、閉じた構造を持つ脂質ベシクル(リポソームと呼ばれる)ができます(水和法、図2a)。まさにフリーズドライのスープにお湯を加えるような、驚くほどの手軽さで分子集合により人工脂質膜小胞ができるのです。ただ、この方法だと膜の形状や層構造が制御されていない様々なリポソームができますので、もっと制御した(サイズがそろっている、膜構造が細胞と同様に1層である、など)ものをつくるための方法も開発されています(文献2, 3、図2b)。
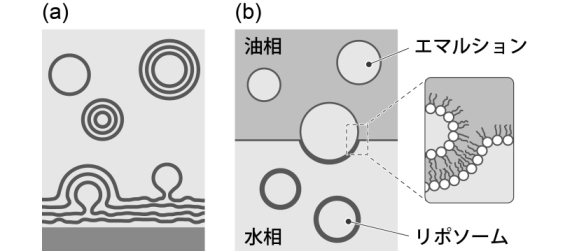
図1 (a) 水和法によるリポソーム形成。(b)Water-in-oilエマルションの界面通過法によりリポソーム形成。分子の内封効率が良い。
では、なぜ水中で疎水性の部分同士が会合するのでしょうか。疎水性部分(主に炭化水素鎖)は電気的な極性を持たないため、それら同士が引力を持つわけではありません。引力を持つのは、周囲にある水分子同士です。すなわち,水分子は水分子と結合していたほうがエネルギー的に安定であり,リン脂質の疎水性部分と隣り合っている水分子は不安定ということになります.その結果,疎水性部分同士が集まったほうが,水と隣り合う総面積が減るため,その状態がエネルギー最安定となります.水分子を安定化するために疎水性分子が集まるのですが,これを疎水性相互作用(疎水性結合)といいます.
また,分子集合では,エントロピー由来の力も重要であることが知られています(文献4).エントロピーとは大学の熱力学や統計力学で習う概念で、ある状態を達成するのに構成される分子配置の多様さ(多重度と呼ぶ)を表すものです。トランプのカードをひくときに、同じマークのカードが多いほどそのマークのカードを引くことが多いのと同じように、ある状態に属する分子の配置の数が多いほど、その状態になりやすいことを示しています。実は、このような確率の原理から、分子やその集合体が結合する「力」が生じるのです(枯渇力と呼ばれます)。皆さんがよくご存知の、理科で習う浸透圧もエントロピーの効果によります。半透膜を介して、純水中の水分子が溶液側に移動して溶液側の体積を増したほうが、溶質の配置の多重度が増えます。高分子も、長いひもの中にあるそれぞれの部分の位置の多重度が最も大きくなるような形状に落ち着きます。細胞中の様々な分子も、系の配置の多重度が大きくなるように変化します。これらの変化は、「力」として現れるのです。私たちは、人工脂質小胞内に封入した高分子のエントロピー増大に伴って、膜が丸まるように変形し、細胞分裂のような現象が起こることを発見しました(図2、文献5,6)。
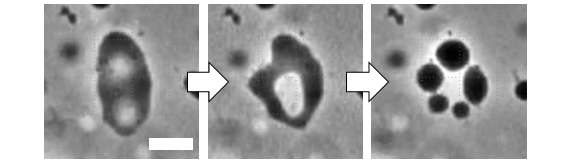
図2 ふにゃふにゃした形状のジャイアントリポソームの膜が曲率を持つように変形し、5個の娘リポソームが数珠状に連結した形状に変化する様子。スケールは5マイクロメートル。
実際には、分子が結合して安定化するという傾向と、分子の配置の多重度が増えるという傾向の2種類が拮抗して、分子集合の状態が決まります(これは自由エネルギーの最小化と呼ばれます)。さらに、特に生命(細胞)で特徴的なのは、エネルギーを消費することによって、自由エネルギーが最小ではない、別の安定状態に分子が集合する現象です(文献8)。この現象は散逸構造というキーワードで語られます。統一した理論がないので、個別の現象ごとに個別に解析されているのが現状です。
■科学的・社会的意義 分子集合は、生物・非生物を問わずナノテクノロジーにおいて最も重要な概念です。ナノスケールの世界では、マクロスケールの物体のように、構成要素を個別に操作して組み立てることができません。本稿ではおおまかな概念のみを示しましたが、分子集合を支配する原理を理解することが、新しい物質や減少、システムを理解したり、作り出したりする際に必須であることは疑いの余地がありません。
■参考文献
1)P. W. K. Rothemund (2006). "Folding DNA to create nanoscale shapes and patterns." Nature 440 (16): 297-302.
2)P. Walde et al. (2010). “Giant Vesicles: Preparations and Applications.” ChemBioChem 11: 848-865.
3)山田、濱田、吉川 (2009). 「細胞サイズの新しい作製法とその応用」生物物理、49 (5): 256-259.
4)R. Phillipsら著、笹井ら訳 (2011).「細胞の物理生物学」、共立出版.
5)H. Terasawa et al. (2012). “Coupling of the fusion and budding of giant phospholipid vesicles containing macromolecules.” Proc. Natl. Acad. Sci. USA 109(16): 5942-5947.
6)H. Shiomi et al. (2014). “Liposome-based liquid handling platform featuring addition, mixing, and aliquoting of femtoliter volumes.” Plos One 9(7): e101820.
7)プリコジン、スタンジェール著、伏見ら訳.「混沌からの秩序」みすず書房.
■良く使用する材料・機器
1)蛍光顕微鏡システム Ti-E (株式会社ニコン)
2)蛍光顕微鏡システム IX-51 (株式会社ニコン)
3)sCMOSカメラ Zyla (アンドール株式会社)
4)共焦点レーザー顕微鏡システム LSM-700 (カールツァイス株式会社)
H28年度分野別専門委員
中央大学・理工学部・精密機械工学科
鈴木宏明(すずきひろあき)
https://www.mech.chuo-u.ac.jp/~suzukilab/
